Hvad sker der, når en sølvske opbevares i vandig opløsning af kobbersulfat?
1. Sølvske bliver brunrød:
* Sølvskeen vil udvikle en rødbrun belægning, da kobbermetal deponeres på dens overflade. Dette skyldes, at sølv er mere reaktiv end kobber.
* Reaktionen er en enkelt forskydningsreaktion, hvor sølv (Ag) fortrænger kobber (Cu) fra kobbersulfatopløsningen.
2. Blå farve på opløsningen falmer:
* Den blå farve på kobbersulfatopløsningen falder gradvist, da kobberionerne (Cu²⁺) reduceres til kobbermetal og afsættes på sølvskeen.
3. Dannelse af sølvioner:
* Når sølv erstatter kobber i opløsningen, frigøres sølvioner (AG⁺) i opløsningen.
Her er den kemiske ligning, der repræsenterer reaktionen:
`` `
2AG (S) + CUSO₄ (AQ) → CU (S) + AG₂SO₄ (AQ)
`` `
Forklaring:
* reaktanter:
* Sølv (AG) - Sølvskeen
* Kobbersulfat (cuso₄) - Den vandige opløsning
* Produkter:
* Kobber (CU) - deponeret på sølvskeen
* Sølvsulfat (ag₂so₄) - opløst i opløsningen
Kortfattet:
Sølvskeen fungerer som et reduktionsmiddel, accepterer elektroner fra kobberioner og bliver belagt med kobbermetal. Kobberionerne mister deres blå farve, når de reduceres, og opløsningen bliver mindre blå. Sølvioner frigøres i opløsningen, hvilket forårsager en ændring i sammensætningen af opløsningen.
 Varme artikler
Varme artikler
-
 Forskere afslører sensor, der hurtigt opdager COVID-19-infektionNår den er knyttet til understøttende elektronik, sensoren kan trådløst overføre data til brugerens mobiltelefon via Bluetooth. Kredit:Caltech Et træk ved COVID-19-virussen, der gør den så vanskel
Forskere afslører sensor, der hurtigt opdager COVID-19-infektionNår den er knyttet til understøttende elektronik, sensoren kan trådløst overføre data til brugerens mobiltelefon via Bluetooth. Kredit:Caltech Et træk ved COVID-19-virussen, der gør den så vanskel -
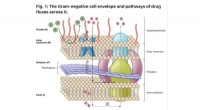 Forskere præsenterer indsigt i søgen efter nye antibiotikaKredit:University of Oklahoma Et samarbejdende forskerhold fra University of Oklahoma, Memorial Sloan Kettering Cancer Center og Merck &Co. offentliggjorde en meningsartikel i tidsskriftet, Natur
Forskere præsenterer indsigt i søgen efter nye antibiotikaKredit:University of Oklahoma Et samarbejdende forskerhold fra University of Oklahoma, Memorial Sloan Kettering Cancer Center og Merck &Co. offentliggjorde en meningsartikel i tidsskriftet, Natur -
 Kemikere ændrer fuldstændig retningen af Diels-Alder-reaktionenOmdannelse af addukter af tangtype til addukter af dominotype med temperaturstigning. Kredit:Fedor Zubkov (illustrationen af Eugenia Lavrova). RUDN-baserede forskere, sammen med russiske kollege
Kemikere ændrer fuldstændig retningen af Diels-Alder-reaktionenOmdannelse af addukter af tangtype til addukter af dominotype med temperaturstigning. Kredit:Fedor Zubkov (illustrationen af Eugenia Lavrova). RUDN-baserede forskere, sammen med russiske kollege -
 Succes med at syntetisere sort fosfor med en sikker og højtydende metode til kunstig fotosynteseSyntetiseret sort fosfor. Kredit:Sakai Chemical Co., Ltd. / Osaka City University En fælles forskergruppe ved Osaka City University og Sakai Chemical Industry Co., Ltd. er lykkedes med at syntetis
Succes med at syntetisere sort fosfor med en sikker og højtydende metode til kunstig fotosynteseSyntetiseret sort fosfor. Kredit:Sakai Chemical Co., Ltd. / Osaka City University En fælles forskergruppe ved Osaka City University og Sakai Chemical Industry Co., Ltd. er lykkedes med at syntetis


