Hvad sker der, når en jernspik er nedsænket i kobbersulfatopløsning?
1. Jern neglen bliver belagt med kobber:
* Jern er mere reaktiv end kobber. Dette betyder, at jernatomer kan fortrænge kobberioner fra opløsningen.
* Jernatomer mister elektroner og bliver jern (II) -ioner (Fe²⁺). Disse ioner opløses derefter i opløsningen.
* Kobberioner (cu²⁺) fra opløsningen får elektroner og bliver kobberatomer, der deponeres på overfladen af jernneglen.
2. Den blå farve på kobbersulfatopløsningen falmer:
* Kobbersulfatopløsning er blå på grund af tilstedeværelsen af kobber (II) -ioner (Cu²⁺).
* Når kobberioner indtages i reaktionen, falmer den blå farve gradvist.
3. Løsningen kan blive grønlig:
* Jern (II) -ioner (Fe²⁺), der er opløst i opløsningen, kan reagere med sulfationer (SO₄²⁻) for at danne jern (II) sulfat, som har en grønlig farve.
Den samlede kemiske reaktion kan repræsenteres som:
Fe (S) + CUSO₄ (AQ) → FESO₄ (AQ) + CU (S)
Kortfattet:
* Jern fortrænger kobber fra opløsningen og belægger neglen med kobber.
* Den blå farve på kobbersulfatopløsningen falmer.
* Opløsningen kan blive grønlig på grund af dannelsen af jern (II) sulfat.
Denne reaktion er et eksempel på en enkelt forskydningsreaktion , hvor et mere reaktivt metal fortrænger et mindre reaktivt metal fra dens forbindelse.
 Varme artikler
Varme artikler
-
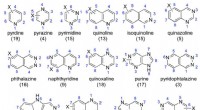 Mod en bedre forståelse af struktur-metabolisme-forhold i human aldehydoxidase (opdatering)Eksempler på de undersøgte azaaromatiske stilladser:antallet af testede forbindelser er angivet i parentes. Kredit:(c) Procedurer fra National Academy of Sciences (2017). DOI:10.1073/pnas.1618881114
Mod en bedre forståelse af struktur-metabolisme-forhold i human aldehydoxidase (opdatering)Eksempler på de undersøgte azaaromatiske stilladser:antallet af testede forbindelser er angivet i parentes. Kredit:(c) Procedurer fra National Academy of Sciences (2017). DOI:10.1073/pnas.1618881114 -
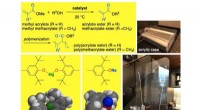 Industriel forbindelse får en miljøvenlig reaktionNatrium- eller magnesiumaryloxider kan katalysere transesterificeringen af methyl(meth)acrylat ved stuetemperatur, med høj kemoselektivitet, producerer et højt udbytte af (meth) acrylatester, og ude
Industriel forbindelse får en miljøvenlig reaktionNatrium- eller magnesiumaryloxider kan katalysere transesterificeringen af methyl(meth)acrylat ved stuetemperatur, med høj kemoselektivitet, producerer et højt udbytte af (meth) acrylatester, og ude -
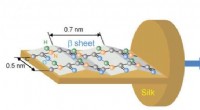 Ny infrarød billeddannelsesteknik afslører molekylær orientering af proteiner i silkefibreOrienteringen af C =O, C-N, og NH-bindinger i amidstruktur af L-sektionen af silkefibre bekræftet i denne undersøgelse af hyper-spektral billeddannelse. Kredit:Australian Synchrotron Et stort
Ny infrarød billeddannelsesteknik afslører molekylær orientering af proteiner i silkefibreOrienteringen af C =O, C-N, og NH-bindinger i amidstruktur af L-sektionen af silkefibre bekræftet i denne undersøgelse af hyper-spektral billeddannelse. Kredit:Australian Synchrotron Et stort -
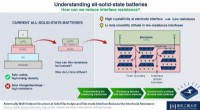 Gør det krystalklart:Krystallinitet reducerer modstanden i all-solid-state batterierKredit:Taro Hitosugi og Tokyo Institute of Technology Forskere ved Tokyo Institute of Technology har undersøgt mekanismerne bag modstanden ved elektrode-elektrolyt-grænsefladen på hel-solid-state
Gør det krystalklart:Krystallinitet reducerer modstanden i all-solid-state batterierKredit:Taro Hitosugi og Tokyo Institute of Technology Forskere ved Tokyo Institute of Technology har undersøgt mekanismerne bag modstanden ved elektrode-elektrolyt-grænsefladen på hel-solid-state
- Hvorfor er biodiversitet vigtig for økosystemer?
- Hvad er en sedimentær klippe, der består af mineralkalkit, der kommer fra fordampede havvand og dy…
- Californien er berømt for jordskælv og skovbrande - men glem ikke dets vulkaner
- Hvad findes bakteriofag lambda i?
- Forbud mod gasdrevne biler virker ikke uden investeringer i infrastruktur, siger ekspert
- Eksponering for vold i hjemmet koster den amerikanske regering 55 milliarder dollars hvert år


