Hvilken ædel gas bliver svovl isoelektronisk med?
Her er hvorfor:
* Svovls elektronkonfiguration: [Ne] 3S² 3P⁴
* Argons elektronkonfiguration: [Ne] 3S² 3P⁶
Ved at få to elektroner fylder svovl sit 3P -underskal og opnår den samme elektronkonfiguration som Argon. Isoelektroniske arter har det samme antal elektroner og derfor lignende kemiske egenskaber.
 Varme artikler
Varme artikler
-
 Færdiggørelse af lægemiddeldesignstikksavenKredit:University of East Anglia En kraftfuld ny måde at analysere, hvordan lægemidler interagerer med molekyler i kroppen, kan hjælpe med at designe bedre behandlinger med færre bivirkninger. De
Færdiggørelse af lægemiddeldesignstikksavenKredit:University of East Anglia En kraftfuld ny måde at analysere, hvordan lægemidler interagerer med molekyler i kroppen, kan hjælpe med at designe bedre behandlinger med færre bivirkninger. De -
 Ny teknologi vil gøre det muligt at fremstille vigtige metaller mere effektivtVed at tilføje kombinationer af kulstof, brint, og iltatomer til stædige, svære at fordampe metaller som wolfram og platin, University of Minnesota Twin Cities forskere var i stand til at omdanne elem
Ny teknologi vil gøre det muligt at fremstille vigtige metaller mere effektivtVed at tilføje kombinationer af kulstof, brint, og iltatomer til stædige, svære at fordampe metaller som wolfram og platin, University of Minnesota Twin Cities forskere var i stand til at omdanne elem -
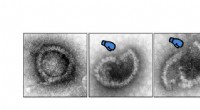 Et skridt på vejen mod bedre behandlinger mod viraEt elektronmikroskopbillede. Det viser, hvordan herpesvirus angribes af proteinet MxB. Kredit:Manutea Serrero &Beate Sodeik, Virology, Hannover Medical School, Tyskland. De fleste celler kan forsva
Et skridt på vejen mod bedre behandlinger mod viraEt elektronmikroskopbillede. Det viser, hvordan herpesvirus angribes af proteinet MxB. Kredit:Manutea Serrero &Beate Sodeik, Virology, Hannover Medical School, Tyskland. De fleste celler kan forsva -
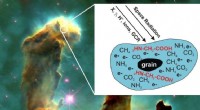 Hvordan livets byggesten kan dannes i rummetElektroner med lav energi skabt i stof af rumstråling (f.eks. galaktiske kosmiske stråler, GCR, etc.), kan inducere dannelse af glycin (2HN-CH2-COOH) i astrofysiske molekylære iser; her, iskolde korn
Hvordan livets byggesten kan dannes i rummetElektroner med lav energi skabt i stof af rumstråling (f.eks. galaktiske kosmiske stråler, GCR, etc.), kan inducere dannelse af glycin (2HN-CH2-COOH) i astrofysiske molekylære iser; her, iskolde korn
- Tre nye RR Lyrae variable stjerner opdaget
- Hvad er mineralsammensætningen af rød jord?
- Sådan løses ukorrekt fraktion Mathproblemer
- Composite metal foam overgår aluminium til brug i flyvinger
- Hjerneskader hos fisk, der er ramt af plastik nanopartikler
- Betelgeuse og Rigel er stjerner, hvor konstellation?


