Hvordan kan to molekyler med den samme kemiske formel reagere forskelligt?
1. Strukturelle isomerer:
* Forskellige arrangementer af atomer: Molekyler med den samme formel, men forskellige arrangementer af atomer kaldes strukturelle isomerer. Disse forskelle i struktur fører til forskellige kemiske egenskaber og reaktivitet. For eksempel findes butan (C4H10) som to strukturelle isomerer:n-butan og isobutan. De har forskellige kogepunkter og reaktivitet på grund af deres forskellige former.
2. Stereoisomerer:
* forskellige rumlige arrangementer: Stereoisomerer har den samme strukturelle formel, men adskiller sig i det tredimensionelle arrangement af deres atomer. Denne forskel kan opstå fra:
* enantiomerer: Ikke-superimposable spejlbilleder af hinanden (som venstre og højre hænder). De udviser ofte forskellige interaktioner med chirale miljøer, som enzymer i biologiske systemer.
* diastereomerer: Stereoisomerer, der ikke er spejlbilleder af hinanden. De har forskellige fysiske og kemiske egenskaber.
3. Funktionelle gruppe isomerer:
* Forskellige funktionelle grupper: Molekyler med den samme formel kan have forskellige funktionelle grupper fastgjort. Funktionelle grupper er specifikke arrangementer af atomer, der påvirker et molekyls reaktivitet. F.eks. Har ethanol (C2H5OH) og dimethylether (CH3OCH3) begge formlen C2H6O, men adskiller sig i deres funktionelle grupper (hydroxylgruppe i ethanol vs. ether -binding i dimethylether), hvilket resulterer i forskellige kemiske adfærd.
4. Konformationelle isomerer:
* Forskellige rotationer omkring enkeltbindinger: Konformationelle isomerer er forskellige rumlige arrangementer af et molekyle, der kan interkonverteres ved rotation omkring enkeltbindinger. Disse konformere har ofte forskellige energier og kan påvirke reaktiviteten, især i reaktioner, der involverer sterisk hindring.
5. Tautomerisme:
* Interconversion gennem protonoverførsel: Tautomerer er isomerer, der interkonverter gennem bevægelsen af en proton. Disse forskellige former kan eksistere i ligevægt, hvilket fører til forskellig reaktivitet.
I resuméet Selvom to molekyler har den samme kemiske formel, kan deres forskellige strukturer, rumlige arrangementer, funktionelle grupper eller dynamiske interkonversioner resultere i betydelige forskelle i deres kemiske opførsel og reaktioner.
 Varme artikler
Varme artikler
-
 Konstruerede defekter i krystallinsk materiale øger den elektriske ydeevneXiaoli Tan og et team af campus-samarbejdspartnere brugte dette transmissionselektronmikroskop på Ames Laboratorys Sensitive Instrument Facility til at studere virkningerne af tekniske defekter i viss
Konstruerede defekter i krystallinsk materiale øger den elektriske ydeevneXiaoli Tan og et team af campus-samarbejdspartnere brugte dette transmissionselektronmikroskop på Ames Laboratorys Sensitive Instrument Facility til at studere virkningerne af tekniske defekter i viss -
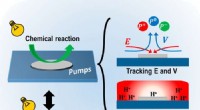 Mikropumper som en platform til forståelse af kemisk drevne mikromotorerKredit:Catalan Institute of Nanoscience and Nanotechnology Udviklingen af selvkørende mikro- og nanomaskiner, der er i stand til at efterligne den menneskelige krops og/eller det naturlige miljø
Mikropumper som en platform til forståelse af kemisk drevne mikromotorerKredit:Catalan Institute of Nanoscience and Nanotechnology Udviklingen af selvkørende mikro- og nanomaskiner, der er i stand til at efterligne den menneskelige krops og/eller det naturlige miljø -
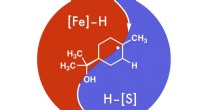 Har du travlt med at udvikle medicin? Her er din chatRice University-forskere udvikler cHAT for at forenkle reduktionen af alkener til mere nyttige mellemmolekyler for lægemidler og andre nyttige kemiske forbindelser. Kredit:West Laboratory/Rice Unive
Har du travlt med at udvikle medicin? Her er din chatRice University-forskere udvikler cHAT for at forenkle reduktionen af alkener til mere nyttige mellemmolekyler for lægemidler og andre nyttige kemiske forbindelser. Kredit:West Laboratory/Rice Unive -
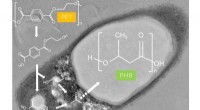 Hvordan en bakterie kan hjælpe med at løse plastikforureningskrisenI. sakaiensis dyrket på poly (ethylenterephthalat) (PET) akkumulerer poly (3-hydroxybutyrat) (PHB). Kredit:Shosuke Yoshida Plastforurening er et af de mest presserende miljøspørgsmål i vores tid.
Hvordan en bakterie kan hjælpe med at løse plastikforureningskrisenI. sakaiensis dyrket på poly (ethylenterephthalat) (PET) akkumulerer poly (3-hydroxybutyrat) (PHB). Kredit:Shosuke Yoshida Plastforurening er et af de mest presserende miljøspørgsmål i vores tid.
- Hvor selv en automatiseret, tilsluttet køretøj kan forbedre sikkerheden og spare energi i trafikke…
- Lanthanid-organiske ramme nanotermometre fremstillet ved spraytørring
- Hold sammen mysteriet om, hvordan enkeltcellede livsformer udviklede sig til flercellede organismer
- Voldelig kriminalitet stiger i varmere vintre
- Kæmpe gasfelter under et koralrev – vil afvisning af miljømæssige årsager stoppe Woodsides Brows…
- Undersøgelse finder filmkritikere, som filmskabere og rollelister, er stort set hvide og mænd


