Hvorfor er natrium kation?
* Elektronkonfiguration: Natrium (NA) har et atomnummer på 11, hvilket betyder, at det har 11 elektroner. Dens elektronkonfiguration er 2, 8, 1. Dette betyder, at den har en elektron i sin yderste skal (Valence Shell).
* octet regel: Atomer har en tendens til at være mest stabile, når de har en fuld ydre skal af elektroner. For de fleste elementer betyder det at have otte elektroner i deres valensskal (oktetreglen).
* mister en elektron: Natrium kan opnå en stabil oktet ved at miste sin enkelt valenselektron. Når det gør dette, bliver det en positivt ladet ion (kation) med den samme elektronkonfiguration som den ædle gas neon (2, 8).
* ionisk binding: Natriums tendens til at miste en elektron gør det meget reaktivt, især med ikke -metaller som klor, som har en stærk tilknytning til elektroner. Natriums tab af en elektron og chlorens forstærkning af en elektron skaber en ionisk binding, der danner natriumchlorid (NaCl), også kendt som bordsalt.
Kortfattet: Natrium bliver en kation (Na+), fordi det let mister en elektron for at opnå en stabil elektronkonfiguration og opfylder oktetreglen.
Sidste artikelHvorfor kan du ikke laboratoriepakke hydrofluorinsyre med vermiculite?
Næste artikelHvilket kendt stof holder varme bedst?
 Varme artikler
Varme artikler
-
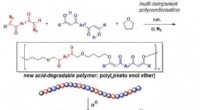 Ny syntetisk polymer nedbrydeligt under meget milde sure betingelserFremstilling af ny nedbrydelig syntetisk polymer. Kredit:Ehime University Et forskerhold ved Ehime University forberedte en ny type syntetisk polymer, som kan nedbrydes til en kombination af velde
Ny syntetisk polymer nedbrydeligt under meget milde sure betingelserFremstilling af ny nedbrydelig syntetisk polymer. Kredit:Ehime University Et forskerhold ved Ehime University forberedte en ny type syntetisk polymer, som kan nedbrydes til en kombination af velde -
 Video:Kamæleoner er mestre i nanoteknologiKredit:The American Chemical Society Kamæleoner er naturens mest talentfulde farvemestre. De bruger deres unikke farveskiftende evner af alle mulige årsager. Men hvordan ændrer de deres farvetone?
Video:Kamæleoner er mestre i nanoteknologiKredit:The American Chemical Society Kamæleoner er naturens mest talentfulde farvemestre. De bruger deres unikke farveskiftende evner af alle mulige årsager. Men hvordan ændrer de deres farvetone? -
 Teamet udvikler metode til neurale netberegninger i vandEt ionisk kredsløb, der omfatter hundredvis af ioniske transistorer. Kredit:Woo-Bin Jung/Harvard SEAS Mikroprocessorer i smartphones, computere og datacentre behandler information ved at manipulere
Teamet udvikler metode til neurale netberegninger i vandEt ionisk kredsløb, der omfatter hundredvis af ioniske transistorer. Kredit:Woo-Bin Jung/Harvard SEAS Mikroprocessorer i smartphones, computere og datacentre behandler information ved at manipulere -
 Det mest detaljerede røntgenbillede af batterier har endnu ikke afsløret, hvorfor de stadig ikke e…Dybdegående beregningsmodeller af kommercielle lithium-ion batterielektroder afslører specifikt, hvor der sker skade ved brug. Kredit:Purdue University billede/Kejie Zhao Elbiler er afhængige af d
Det mest detaljerede røntgenbillede af batterier har endnu ikke afsløret, hvorfor de stadig ikke e…Dybdegående beregningsmodeller af kommercielle lithium-ion batterielektroder afslører specifikt, hvor der sker skade ved brug. Kredit:Purdue University billede/Kejie Zhao Elbiler er afhængige af d
- Hvad er adaptivt tøj, og hvordan kan det gøre livet lettere for mennesker med et handicap?
- Sådan ændrer du verden:Nyt arbejdspapir analyserer ledere fremmer udvikling
- Hvordan man forbereder en glukoseopløsning
- Gå ikke ud fra, at sprog eller dialekt er låst til et bestemt sted
- Billeder og gestus er effektive støttemetoder i fremmedsprogsundervisningen for børn
- Fremskridt med atomkraftmikroskop fører til ny brystkræftforskning


