Hvor mange elektroner i en jordtilstands telluriumatom er orbitaler mærket af L er lig med 1?
1. Bestem elektronkonfigurationen
* Tellurium (TE) har et atomnummer på 52, hvilket betyder, at det har 52 elektroner.
* Elektronkonfigurationen for Tellurium er:1S² 2S² 2P⁶ 3S² 3P⁶ 4S² 3D¹⁰ 4P⁶ 5S² 4D¹⁰ 5P⁴
2. Forstå forholdet mellem L og Subshells
* Kvantetal * l * repræsenterer vinkelmoment af en elektron og definerer formen på dets orbital.
* * l * =0 svarer til en S Orbital (sfærisk)
* * l * =1 svarer til en p orbital (håndvægtformet)
* * l * =2 svarer til en d orbital (mere kompleks form)
3. Identificer P -underskaller
* I elektronkonfigurationen er underskallerne med * l * =1 p -underskaller: 2p, 3p, 4p og 5p.
4. Tæl elektronerne i P -underskaller
* 2p:6 elektroner
* 3P:6 elektroner
* 4P:6 elektroner
* 5p:4 elektroner
5. Beregn det samlede
* Tilføj elektronerne fra alle P -underskaller:6 + 6 + 6 + 4 = 22 elektroner
Derfor er der 22 elektroner i et jordtilstands telluriumatom med en * l * værdi på 1.
Sidste artikelEr det at gøre is til en kemisk eller fysisk forandring?
Næste artikelBruger fotosyntesen kuldioxid og vand som reaktant?
 Varme artikler
Varme artikler
-
 I glødende farver:At se spredningen af narkotikapartikler i et retsmedicinsk laboratoriumNIST-forskere brugte glødende pulver til at forstå, hvordan lægemiddelpartikler kan spredes på overflader i et retskemisk laboratorium. Kredit:E. Sisco, M. Staymates/NIST Da to videnskabsmænd fra
I glødende farver:At se spredningen af narkotikapartikler i et retsmedicinsk laboratoriumNIST-forskere brugte glødende pulver til at forstå, hvordan lægemiddelpartikler kan spredes på overflader i et retskemisk laboratorium. Kredit:E. Sisco, M. Staymates/NIST Da to videnskabsmænd fra -
 Høj præcision, analyse på stedet af ædle metaller i spild af metallurgisk affaldPrøve introduktion i LepiCube-C og måling i LEP-OES. Kredit:Kanazawa University Ædelmetaller er begrænsede ressourcer i høj efterspørgsel. De opnås hovedsageligt gennem minedrift, men forskere und
Høj præcision, analyse på stedet af ædle metaller i spild af metallurgisk affaldPrøve introduktion i LepiCube-C og måling i LEP-OES. Kredit:Kanazawa University Ædelmetaller er begrænsede ressourcer i høj efterspørgsel. De opnås hovedsageligt gennem minedrift, men forskere und -
 Ny biosensor stimulerer sved, mens patienten er kølig og hvilerUC udviklede en ny biosensor, der stimulerer sved på et lille stykke hud. Kredit:Andrew Higley/UC Creative Services En ulempe ved medicinske sensorer, der tester menneskelig sved:Du skal svede.
Ny biosensor stimulerer sved, mens patienten er kølig og hvilerUC udviklede en ny biosensor, der stimulerer sved på et lille stykke hud. Kredit:Andrew Higley/UC Creative Services En ulempe ved medicinske sensorer, der tester menneskelig sved:Du skal svede. -
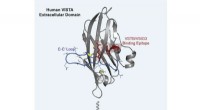 Ny indsigt i et kræftbeskyttende protein kan guide en ny generation af kræftbehandlingerVed hjælp af en kombination af beregning og eksperiment, forskere var i stand til at kortlægge formen på VISTA, et checkpoint protein, der forsvarer kræftceller mod immunsystemangreb, samt den del af
Ny indsigt i et kræftbeskyttende protein kan guide en ny generation af kræftbehandlingerVed hjælp af en kombination af beregning og eksperiment, forskere var i stand til at kortlægge formen på VISTA, et checkpoint protein, der forsvarer kræftceller mod immunsystemangreb, samt den del af
- Hvad er tilstanden af materie mest ikke -metaller?
- Forskere opbygger modstandskraft midt i det kogende vand
- Hvad menes med arbejdsdeling i en multicellulær organisme?
- Beskriv topografien på havbunden?
- Nøjagtig kortlægning af menneskelige rejsemønstre med globale smartphonedata
- Virksomheder balancerer Facebooks privatlivsbekymringer, annoncebehov


