Giv bevis for at støtte ideen om, at stoffer består af partikler?
1. Diffusion og brownisk bevægelse:
* diffusion: Den gradvise spredning af et stof gennem et medium (som en dråbe madfarve i vand). Dette forklares med den tilfældige bevægelse af partikler, der kolliderer og spreder sig.
* brownisk bevægelse: Den uberegnelige, vridende bevægelse af små partikler suspenderet i en væske (som pollenkorn i vand). Denne bevægelse er forårsaget af kollisioner med de usynlige partikler af væsken, hvilket demonstrerer deres eksistens.
2. Stater med stof:
* faste stoffer: Partikler er tæt pakket og vibrerer i faste positioner. Dette forklarer deres stive struktur og manglende evne til at flyde.
* væsker: Partikler er tættere sammen end i gasser, men kan bevæge sig rundt i hinanden. Dette forklarer deres evne til at flyde og tage formen på deres beholder.
* Gasser: Partikler er langt fra hinanden og bevæger sig frit og tilfældigt. Dette forklarer deres kompressibilitet og evne til at fylde enhver beholder.
3. Kemiske reaktioner:
* Lov om bevarelse af masse: I en kemisk reaktion svarer den samlede masse af reaktanter den samlede masse af produkter. Dette forklares ved omarrangement af atomer (partikler) under reaktionen, ikke deres ødelæggelse eller skabelse.
* støkiometri: De faste forhold mellem reaktanter og produkter i kemiske reaktioner (f.eks. 2 hydrogenatomer + 1 iltatom =1 vandmolekyle) forklares ved kombination af specifikt antal partikler.
4. Fysiske egenskaber:
* kogepunkt: Temperaturen, hvorpå et stof skifter fra væske til gas. Dette forklares af, at partiklerne får nok energi til at overvinde intermolekylære kræfter, der holder dem sammen.
* smeltepunkt: Temperaturen, hvorpå et stof skifter fra fast til væske. Dette forklares af, at partiklerne får nok energi til at overvinde de faste positioner, de havde i fast tilstand.
5. Atomteori:
* Daltons atomteori: Foreslog, at elementer består af små, udelelige partikler kaldet atomer. Dette lagde grundlaget for ideen om partikler som de grundlæggende byggesten til stof.
* moderne atomteori: Forklarer strukturen af atomer med protoner, neutroner og elektroner, hvilket yderligere størkning af materiens partikel -karakter.
Disse beviser antyder kraftigt, at stoffer er sammensat af partikler. Selvom vi ikke direkte kan observere individuelle partikler med det blotte øje, forklarer disse partiklers kollektive opførsel en lang række fænomener, vi oplever i den makroskopiske verden.
 Varme artikler
Varme artikler
-
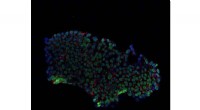 Starten på en ny æra inden for stamcelleterapiKredit:Koc University En nylig undersøgelse offentliggjort i 8. april-udgaven af Naturens kemiske biologi forbedrer metoden Cellular Reprogramming udviklet af Nobelpristageren i medicin og fysio
Starten på en ny æra inden for stamcelleterapiKredit:Koc University En nylig undersøgelse offentliggjort i 8. april-udgaven af Naturens kemiske biologi forbedrer metoden Cellular Reprogramming udviklet af Nobelpristageren i medicin og fysio -
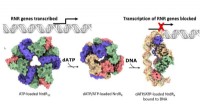 Ny mekanisme til regulering af forsyningen af DNA-byggesten til bedre antibiotikaVirkningsmekanismen af den RNR-specifikke repressor NrdR. Overfladerepræsentation af cryo-EM-kortene for de dodecameriske, oktamere og DNA-bundne tetramere NrdR-strukturer. NrdR-monomerer i hver tet
Ny mekanisme til regulering af forsyningen af DNA-byggesten til bedre antibiotikaVirkningsmekanismen af den RNR-specifikke repressor NrdR. Overfladerepræsentation af cryo-EM-kortene for de dodecameriske, oktamere og DNA-bundne tetramere NrdR-strukturer. NrdR-monomerer i hver tet -
 Bioinspirerede materialer fra mælkebøtterLuftindkapslende elastiske mekanisme af nedsænkede Taraxacum-blæsebolde. Kredit:University of Trento Marker er dækket af mælkebøtter om foråret, en meget almindelig plante med gul-guld blomster og
Bioinspirerede materialer fra mælkebøtterLuftindkapslende elastiske mekanisme af nedsænkede Taraxacum-blæsebolde. Kredit:University of Trento Marker er dækket af mælkebøtter om foråret, en meget almindelig plante med gul-guld blomster og -
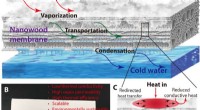 Ny træmembran giver et bæredygtigt alternativ til vandfiltreringSkematisk af processen med brug af den nye træmembran til destillering af vand. Kredit:T. Li, University of Maryland. Inspireret af det indviklede vandsystem, der cirkulerer i et træ, et team af f
Ny træmembran giver et bæredygtigt alternativ til vandfiltreringSkematisk af processen med brug af den nye træmembran til destillering af vand. Kredit:T. Li, University of Maryland. Inspireret af det indviklede vandsystem, der cirkulerer i et træ, et team af f
- Trænger undervisning og kommunikation om mikrofluidiske fremskridt til forbedring?
- Hvilken type atmosfære er til stede?
- Forskere lægger en plan for håndtering af floder for klimaændringer
- Økonomi ved en fire-dages arbejdsuge:Forskning viser, at det kan spare virksomheder penge
- Quantum Maxwells dæmon teleporterer entropi ud af en qubit
- Hvordan forener Gene oprindeligt sine handlinger i træet?


