Hvad er den enkelte forskydningsreaktion af Mg plus H2CO3?
mg (s) + h₂co₃ (aq) → mgco₃ (s) + h₂ (g)
Her er en sammenbrud af reaktionen:
* magnesium (mg) er et mere reaktivt metal end brint (H).
* kulsyre (h₂co₃) er en svag syre.
* magnesiumcarbonat (MGCO₃) er et uopløseligt salt.
* brintgas (H₂) produceres som et biprodukt.
Forklaring:
Magnesium fortrænger brint fra kulsyre, fordi det er mere reaktivt. Reaktionen producerer magnesiumcarbonat, som er et fast bundfald, og brintgas, der bobler ud af opløsningen.
Vigtig note: Kulsyre er ustabil og nedbrydes let i kuldioxid (CO₂) og vand (H₂O). Så den faktiske reaktion i opløsning er sandsynlig:
mg (s) + co₂ (aq) + h₂o (l) → mgco₃ (s) + h₂ (g)
Imidlertid er den indledende ligning ved anvendelse af kulsyre en almindelig måde at repræsentere reaktionen på.
Sidste artikelEr organisk opløsningsmiddel et oxidationsmiddel?
Næste artikelHvad er den elektroniske geometri af BCL3 ind i molekyle.?
 Varme artikler
Varme artikler
-
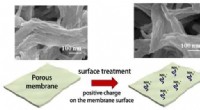 Udvikling af ultratynd holdbar membran til effektiv olie- og vandseparationFigur 1:SEM-billeder og diagram, der viser dannelsen af det ultratynde silicalag på den porøse membran. Kredit:Kobe University Forskere ledet af professor Matsuyama Hideto og professor Yoshioka
Udvikling af ultratynd holdbar membran til effektiv olie- og vandseparationFigur 1:SEM-billeder og diagram, der viser dannelsen af det ultratynde silicalag på den porøse membran. Kredit:Kobe University Forskere ledet af professor Matsuyama Hideto og professor Yoshioka -
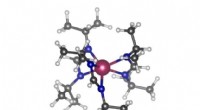 Ny kernemagnetisk resonansspektroskopi-forskning afslører dynamikken af katalysatorer i 3D-rumKredit: Uorganisk kemi grænser (2020). DOI:10.1039/D0QI01241F Forskere fra det amerikanske energiministeriums Ames Laboratory har kortlagt dynamikken i en katalysators aktive sted i tre dimension
Ny kernemagnetisk resonansspektroskopi-forskning afslører dynamikken af katalysatorer i 3D-rumKredit: Uorganisk kemi grænser (2020). DOI:10.1039/D0QI01241F Forskere fra det amerikanske energiministeriums Ames Laboratory har kortlagt dynamikken i en katalysators aktive sted i tre dimension -
 AI-drevet elektronisk næse til at opsnuse kødets friskhedE-næsen indeholder en stregkode, der ændrer farve på grund af reaktioner med gasser, der udsendes af det henfaldende kød, og en stregkodelæser i form af en smartphone-app drevet af AI, og er blevet tr
AI-drevet elektronisk næse til at opsnuse kødets friskhedE-næsen indeholder en stregkode, der ændrer farve på grund af reaktioner med gasser, der udsendes af det henfaldende kød, og en stregkodelæser i form af en smartphone-app drevet af AI, og er blevet tr -
 Stand-up poser fra vedvarende råvarer og nanocelluloseKredit:Technical Research Center of Finland (VTT) VTT Technical Research Center of Finland Ltd har udviklet lette 100% biobaserede stand-up poser med høj teknisk ydeevne. Høj ydeevne i både ilt, f
Stand-up poser fra vedvarende råvarer og nanocelluloseKredit:Technical Research Center of Finland (VTT) VTT Technical Research Center of Finland Ltd har udviklet lette 100% biobaserede stand-up poser med høj teknisk ydeevne. Høj ydeevne i både ilt, f
- Ny forskning om bedrageriske stjerner kan forbedre astronomiske data
- Cloud radar simulator bygger bro mellem klimamodeller og feltdata
- Hvor hurtigt drejer jorden sig i Sacramento?
- Hvilken gas af følgende vil have største afvigelse fra ideel opførsel H2 F2 BR2 og CL2?
- Undersøgelse afslører, hvorfor sangfugle varierer i tid afsat til at varme æg
- Små arktiske kystvandområder, med stor kulstoffrigivelse


