Er organisk opløsningsmiddel et oxidationsmiddel?
Hvad er oxidationsmidler?
* Oxideringsmidler er stoffer, der får elektroner under en kemisk reaktion.
* De får et andet stof til at miste elektroner, der kaldes oxidation.
Kan organiske opløsningsmidler oxideres midler?
* ja, nogle kan. Visse organiske opløsningsmidler indeholder funktionelle grupper eller strukturer, der gør dem i stand til at acceptere elektroner og således fungere som oxidationsmidler. Eksempler inkluderer:
* kromsyre (h₂cro₄): Brugt i nogle oxidationsreaktioner i organisk kemi.
* kaliumpermanganat (kmno₄): Et kraftfuldt oxidationsmiddel, der ofte bruges i organisk syntese.
* hydrogenperoxid (H₂O₂): Brugt i forskellige oxidationsreaktioner, herunder oxidation af alkoholer til aldehyder eller ketoner.
* nej, de fleste er ikke. Mange organiske opløsningsmidler er inerte mod oxidationsreaktioner. De får ikke let elektroner og bruges primært som reaktionsmedier eller til at opløse reaktanter. Eksempler inkluderer:
* hexan: Et ikke -polært opløsningsmiddel anvendt til ekstraktion af ikke -polære forbindelser.
* diethylether: Et almindeligt opløsningsmiddel anvendt i organisk syntese.
* dichlormethan (ch₂cl₂): Et relativt polært opløsningsmiddel anvendt til forskellige reaktioner.
Nøglefaktorer, der skal overvejes:
* Funktionelle grupper: Opløsningsmidler, der indeholder grupper som ketoner, aldehyder eller peroxider, er mere tilbøjelige til at oxidere midler.
* reaktivitet: Det specifikke organiske opløsningsmiddel og betingelserne (temperatur, tilstedeværelse af katalysatorer) kan påvirke dets oxidationspotentiale.
Kortfattet:
Mens nogle organiske opløsningsmidler kan fungere som oxidationsmidler, er flertallet inerte og deltager ikke let i oxidationsreaktioner. For at bestemme, om et specifikt opløsningsmiddel er et oxidationsmiddel, skal du overveje dets struktur, funktionelle grupper og reaktivitet.
 Varme artikler
Varme artikler
-
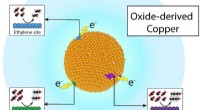 Kulbrændstoffer bliver grønne for vedvarende energiForskere ved Berkeley Lab og Joint Center for Artificial Photosynthesis har vist, at genanvendelse af kuldioxid til værdifulde kemikalier, såsom ethylen og propanol, og brændstoffer som ethanol, kan v
Kulbrændstoffer bliver grønne for vedvarende energiForskere ved Berkeley Lab og Joint Center for Artificial Photosynthesis har vist, at genanvendelse af kuldioxid til værdifulde kemikalier, såsom ethylen og propanol, og brændstoffer som ethanol, kan v -
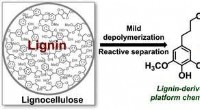 Gør træ til farmaceutiske ingredienserKredit:American Chemical Society Produktion af farligt affald under lægemiddelfremstilling er en alvorlig bekymring for medicinalindustrien. Typisk, store mængder brandfarlige opløsningsmidler anv
Gør træ til farmaceutiske ingredienserKredit:American Chemical Society Produktion af farligt affald under lægemiddelfremstilling er en alvorlig bekymring for medicinalindustrien. Typisk, store mængder brandfarlige opløsningsmidler anv -
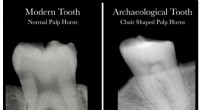 Videnskab møder arkæologi med opdagelsen af, at tandrøntgenstråler afslører D-vitaminmangelSammenligning af tandrøntgenbilleder fra patienter med og uden D-vitaminmangel. Kredit:McMaster University Menneskelige tænder rummer vital information om D-vitaminmangel, en alvorlig, men ofte sk
Videnskab møder arkæologi med opdagelsen af, at tandrøntgenstråler afslører D-vitaminmangelSammenligning af tandrøntgenbilleder fra patienter med og uden D-vitaminmangel. Kredit:McMaster University Menneskelige tænder rummer vital information om D-vitaminmangel, en alvorlig, men ofte sk -
 Hvordan formen påvirker en chokoladebars krystallinske strukturChokoladeforme påvirker chokoladens krystallinske struktur. Kredit:Popovphoto/Shutterstock.com Når du nyder en chokoladebar, de fleste mennesker tænker ikke over, hvordan molekylerne i det er orga
Hvordan formen påvirker en chokoladebars krystallinske strukturChokoladeforme påvirker chokoladens krystallinske struktur. Kredit:Popovphoto/Shutterstock.com Når du nyder en chokoladebar, de fleste mennesker tænker ikke over, hvordan molekylerne i det er orga
- Ny funktion fundet i energispektret af universets mest kraftfulde partikler
- Nogle - men ikke alle - koraller tilpasser sig det varme klima
- Stinging Insects That Nest i Ground
- Opskriften på stjerneklynger:Tag en gassky 500 lysår i diameter, tilføj 5 millioner år, proces i…
- 4 hovedklasser af kulstofforbindelser?
- Forskere udvikler nye nær-ultraviolette LED-eksciterbare nær-infrarøde emittere


