Hvad gør partikler i en væske?
* Luk sammen: Flydende partikler er meget tættere sammen end gaspartikler, men ikke så tæt pakket som faste partikler. Dette er grunden til, at væsker har et fast volumen, men ikke en fast form.
* fri bevægelighed: I modsætning til faste stoffer, hvor partikler er låst på plads, kan flydende partikler bevæge sig rundt i hinanden. Dette forklarer, hvorfor væsker kan flyde og tage formen på deres beholder.
* vibrationsbevægelse: Ligesom partikler i faste stoffer vibrerer flydende partikler konstant. Denne bevægelse er mere kraftig i væsker end faste stoffer.
* attraktive kræfter: Partiklerne i en flydende oplevelse attraktive kræfter og holder dem sammen. Disse kræfter er svagere end i faste stoffer, hvilket giver mulighed for bevægelse, men stadig holder partiklerne relativt tæt.
Her er nogle nøglepunkter om flydende partikler:
* Højere energi end faste stoffer: Partiklerne i en væske har mere energi end partiklerne i et fast stof. Dette giver dem mulighed for at overvinde nogle af de attraktive kræfter, der holder dem sammen.
* diffusion: Væsker kan diffundere, hvilket betyder, at partikler kan bevæge sig fra områder med høj koncentration til områder med lav koncentration. Dette er langsommere end diffusion i gasser.
* Kompressibilitet: Væsker er kun lidt komprimerbare, hvilket betyder, at det er vanskeligt at presse dem ind i et mindre volumen. Dette skyldes, at partiklerne allerede er tæt på hinanden.
Fortæl mig, hvis du gerne vil dykke dybere ned i nogen af disse aspekter!
Sidste artikelHvilket organisk molekyle er mest rigeligt?
Næste artikelHvad kaldes molekyler af identiske monomerer?
 Varme artikler
Varme artikler
-
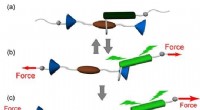 Nysgerrige sammenlåste molekyler viser dobbelt responsFigur 1. Skematisk illustration af driften af en rotaxan-baseret mekanophor, viser (a) kraftfri tilstand, (b) reversibel, og (c) irreversible svar. Forskere udforskede en mærkelig sammenkoblet molek
Nysgerrige sammenlåste molekyler viser dobbelt responsFigur 1. Skematisk illustration af driften af en rotaxan-baseret mekanophor, viser (a) kraftfri tilstand, (b) reversibel, og (c) irreversible svar. Forskere udforskede en mærkelig sammenkoblet molek -
 At få fermenterede mejeriprodukter til at smage bedreEmmental ost. Kredit:Wikipedia Forskere ved det tekniske universitet i München (TUM), Leibniz-instituttet for fødevaresystembiologi, og University of Hohenheim har udviklet en ny metodisk tilgang
At få fermenterede mejeriprodukter til at smage bedreEmmental ost. Kredit:Wikipedia Forskere ved det tekniske universitet i München (TUM), Leibniz-instituttet for fødevaresystembiologi, og University of Hohenheim har udviklet en ny metodisk tilgang -
 Rapid DNA identificerer ofre for undfangelsesbådbrandKredit:U.S. Department of Homeland Security 34 mennesker døde i en tragisk bådbrand den 2. september. 2019, ud for Santa Cruz Islands kyst, Californien. Fem besætningsmedlemmer slap med skader eft
Rapid DNA identificerer ofre for undfangelsesbådbrandKredit:U.S. Department of Homeland Security 34 mennesker døde i en tragisk bådbrand den 2. september. 2019, ud for Santa Cruz Islands kyst, Californien. Fem besætningsmedlemmer slap med skader eft -
 Skaler til nye højder med gekko-inspireret klæbemiddelKredit:American Chemical Society Nogle dyr, såsom gekkoer, kan nemt klatre op ad vægge og på tværs af lofter. Men pt. Der findes ikke noget materiale, der gør det muligt for almindelige mennesker
Skaler til nye højder med gekko-inspireret klæbemiddelKredit:American Chemical Society Nogle dyr, såsom gekkoer, kan nemt klatre op ad vægge og på tværs af lofter. Men pt. Der findes ikke noget materiale, der gør det muligt for almindelige mennesker
- Steder, hvor tektoniske plader mødes?
- Hvad sker der, når fortyndet svovlsyre hældes på kobberplade?
- Forskere udvikler 3D-printbart materiale, der efterligner biologiske væv
- Matematik kaster lys over, hvad forsinkelser i at blive gravid betyder for udsigterne til at få en …
- Se hvordan korngrænser ændrer sig i et metal
- Hvilket navn metalblanding i guld?


