Hvorfor arbejder kemiker med mol af individuelle atomer?
1. Atomer er utroligt små: Atomer er små partikler, og deres individuelle masser er ekstremt små (målt i atommasseenheder, AMU). At arbejde med den faktiske masse af et enkelt atom ville være utroligt besværligt og upraktisk for de fleste beregninger.
2. Moles giver en konsistent og skalerbar enhed: Molen (mol) er en enhed, der repræsenterer et specifikt antal partikler (6,022 x 10^23, også kendt som Avogadros nummer). Dette gør det til en meget mere håndterbar enhed til håndtering af det store antal atomer og molekyler involveret i kemiske reaktioner.
3. Moles relaterer direkte til masse: En mol af ethvert stof har en masse lig med dets atom- eller molekylvægt i gram. Dette forhold gør det nemt at konvertere mellem gram og mol, hvilket er vigtigt for mange kemiske beregninger.
4. Kemiske reaktioner er baseret på forhold: Kemiske reaktioner forekommer i specifikke proportioner mellem reaktanter og produkter. Ved hjælp af moler giver kemikere mulighed for at udtrykke disse proportioner på en klar og kortfattet måde, hvilket gør det lettere at forudsige mængden af de dannede produkt eller reaktanter, der er nødvendige for en given reaktion.
Her er en analogi: Forestil dig at bage en kage. Du kan bruge en lille målingsske til at måle hvert individuelt sukkerkorn, men det ville være kedeligt og upraktisk. I stedet bruger du en større enhed som kopper eller gram til at repræsentere den nødvendige mængde sukker, hvilket er meget mere praktisk og effektivt. Moles er som "kopper" eller "gram" af kemi, der giver en praktisk enhed til at arbejde med store mængder atomer og molekyler.
Sidste artikelHvordan danner en krystal krystal?
Næste artikelEr syrer fra planter rødder, der bryder klipper en mekanisk reaktion?
 Varme artikler
Varme artikler
-
 Var ursuppen en solid pre-protein gryderet?De første livspolymerer kan være opstået ved en daglig proces, der stadig observeres på Jorden i dag, såsom gentagen tørring og genopfyldning af damvand. Kredit:Ram Krishnamurthy / Center for Chemical
Var ursuppen en solid pre-protein gryderet?De første livspolymerer kan være opstået ved en daglig proces, der stadig observeres på Jorden i dag, såsom gentagen tørring og genopfyldning af damvand. Kredit:Ram Krishnamurthy / Center for Chemical -
 Nyt materiale kan generere brint fra salt og forurenet vandKredit:Tomsk Polytechnic University Forskere ved Tomsk Polytechnic University sammen med teams fra University of Chemistry and Technology, Prag og Jan Evangelista Purkyne Universitet i Ústí nad La
Nyt materiale kan generere brint fra salt og forurenet vandKredit:Tomsk Polytechnic University Forskere ved Tomsk Polytechnic University sammen med teams fra University of Chemistry and Technology, Prag og Jan Evangelista Purkyne Universitet i Ústí nad La -
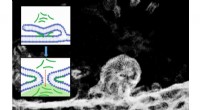 Hvordan trænger peptider ind i celler? To sider af samme møntElektronmikroskopibillede af en todelt cellemembran og det tilsvarende molekylære skema for processen. Kredit:@ IOCB Prag Den simple transport af lægemidler direkte ind i cellerne er et af de prim
Hvordan trænger peptider ind i celler? To sider af samme møntElektronmikroskopibillede af en todelt cellemembran og det tilsvarende molekylære skema for processen. Kredit:@ IOCB Prag Den simple transport af lægemidler direkte ind i cellerne er et af de prim -
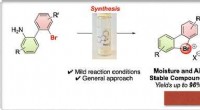 Cykliske hypervalente brom virker som aryne forstadierKredit:Wiley Diaryl λ 3 -bromaner er en sjælden og generelt uforsket klasse af forbindelser. En mild og effektiv protokol leverer nu en bred palet af disse interessante byggesten til organisk sy
Cykliske hypervalente brom virker som aryne forstadierKredit:Wiley Diaryl λ 3 -bromaner er en sjælden og generelt uforsket klasse af forbindelser. En mild og effektiv protokol leverer nu en bred palet af disse interessante byggesten til organisk sy
- Organiske 2-oxocarboxylsyrer giver forbindelse til dannelse af radikaler og reaktive iltarter i atmo…
- Neutroner afslører kvantetunnelering på grafen, hvilket muliggør fødslen af stjerner
- De revolutionerende teknologier, der driver og køler Parker Solar Probe
- Ugunstige holdninger til genetisk modificeret mad forudsiger negative følelser om andre fødevarete…
- Hvordan ser culumonimbus skyer ud?
- At danne tro på en verden af filterbobler


