Hvilke hydrofile stoffer er lavet af?
Her er en sammenbrud af, hvad der gør et stofhydrofil:
polære grupper:
* hydroxylgrupper (-oh): Fundet i alkoholer, sukkerarter og mange andre organiske molekyler.
* carboxylgrupper (-cooh): Fundet i carboxylsyrer og aminosyrer.
* aminogrupper (-nh2): Fundet i aminosyrer og amider.
* phosphatgrupper (-po4): Fundet i nukleinsyrer og phospholipider.
* sulfatgrupper (-SO4): Fundet i nogle proteiner og kulhydrater.
Hvordan disse grupper fungerer:
* Polaritet: Disse grupper er polære, hvilket betyder, at de har en ujævn fordeling af elektroner, hvilket skaber delvis positive og negative afgifter. Vand er også et polært molekyle.
* Hydrogenbinding: De delvise positive ladninger på disse grupper kan danne brintbindinger med de delvise negative ladninger på vandmolekyler.
Eksempler på hydrofile stoffer:
* sukker: Ligesom glukose og fruktose, har mange hydroxylgrupper.
* Proteiner: Indeholder aminosyrer med polære sidekæder.
* DNA og RNA: Nukleinsyrer indeholder phosphatgrupper og andre polære komponenter.
* salte: Dissocier i ioner i vand, der tiltrækkes af de polære vandmolekyler.
Vigtig note: Tilstedeværelsen af polære grupper garanterer ikke fuldstændig opløselighed i vand. Den overordnede struktur og størrelse af molekylet spiller også en rolle. For eksempel kan nogle store molekyler med mange polære grupper stadig kun være delvist opløselige.
I modsætning til hydrofile stoffer, hydrofobe stoffer er lavet af molekyler, der mangler polære grupper og afvises af vand. Disse er typisk ikke -polære molekyler som fedt og olier.
 Varme artikler
Varme artikler
-
 Passer én størrelse alle? En ny model for organiske halvledereRepræsentation af bærermobilitet i hårde uorganiske materialer (øverste figur, båndtransport) og fleksible organiske faste stoffer (nedre tal, fleksibilitetsinduceret transportmekanisme). Kredit:Kazuy
Passer én størrelse alle? En ny model for organiske halvledereRepræsentation af bærermobilitet i hårde uorganiske materialer (øverste figur, båndtransport) og fleksible organiske faste stoffer (nedre tal, fleksibilitetsinduceret transportmekanisme). Kredit:Kazuy -
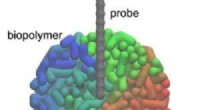 Simulering af 3D-AFM-billeder for systemer, der ikke er i ligevægtKredit:Kanazawa University Forskere ved Kanazawa University rapporterer i Journal of Physical Chemistry Letters hvordan man simulerer 3D atomic force mikroskopi billeder af ude af ligevægt systemer
Simulering af 3D-AFM-billeder for systemer, der ikke er i ligevægtKredit:Kanazawa University Forskere ved Kanazawa University rapporterer i Journal of Physical Chemistry Letters hvordan man simulerer 3D atomic force mikroskopi billeder af ude af ligevægt systemer -
 Sporing af en løsningsproces trin for trinVed hjælp af lavtemperatur scanning tunneling mikroskopi, Karsten Lucht og Karina Morgenstern kan observere individuelle molekylers adfærd i detaljer. Kredit:RUB, Marquard Kemikere fra Ruhr-Univer
Sporing af en løsningsproces trin for trinVed hjælp af lavtemperatur scanning tunneling mikroskopi, Karsten Lucht og Karina Morgenstern kan observere individuelle molekylers adfærd i detaljer. Kredit:RUB, Marquard Kemikere fra Ruhr-Univer -
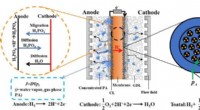 Forudsigelse af fordeling af phosphorsyre og vand i højtemperatur polymerelektrolytmembranbrændsel…Skematisk af katodekatalysatorlaget baseret på agglomerat-antagelsen. Kredit:Sun Mu Højtemperatur polymer elektrolytmembran brændselscelle (HT-PEMFC) kan anvendes i elektriske køretøjer og marine s
Forudsigelse af fordeling af phosphorsyre og vand i højtemperatur polymerelektrolytmembranbrændsel…Skematisk af katodekatalysatorlaget baseret på agglomerat-antagelsen. Kredit:Sun Mu Højtemperatur polymer elektrolytmembran brændselscelle (HT-PEMFC) kan anvendes i elektriske køretøjer og marine s
- NASA ser Mauritius dækket af den tropiske storm Calvinia
- Kunne en super slange dukke op fra Everglades pythoner? Nyt DNA-studie giver mulighed
- Laserbaseret prototype sonderer koldatoms dynamik
- Seksuel chikane er udbredt på mange afrikanske mediearbejdspladser
- Hvilken planet har en solnedgang i øst?
- STEM-superstjerner efterlyser mere køns- og kulturel mangfoldighed


