Hvad observeres, når Fe2SO4 og FESO4.7H2O opvarmes stærkt?
Her er hvad der sker, når disse forbindelser opvarmes kraftigt:
feso₄ · 7H₂O (jern (II) sulfat heptahydrat)
* dehydrering: Efter opvarmning mister heptahydratet sit vand af krystallisation. Følgende reaktion opstår:
Feso₄ · 7H₂O (S) → Feso₄ (S) + 7H₂O (G)
* Nedbrydning: Yderligere opvarmning af den vandfri feso₄ fører til dens nedbrydning:
2Feso₄ (S) → Fe₂o₃ (S) + SO₂ (G) + SO₃ (G)
* observationer: Du vil observere følgende:
* De blågrønne krystaller af feso₄ · 7H₂o bliver hvidt, når vandet fordamper.
* Det hvide faste stof nedbrydes yderligere og bliver brunt som Fe₂o₃₃ (Iron (III) oxid) former.
* Du vil lugte svovldioxid (SO₂) gas, som har en skarp lugt.
feso₄ (vandfri jern (II) sulfat)
* Nedbrydning: Vandfri feso₄ nedbrydes direkte ved stærk opvarmning efter den samme reaktion som ovenfor:
2Feso₄ (S) → Fe₂o₃ (S) + SO₂ (G) + SO₃ (G)
* observationer:
* Det hvide faste stof bliver brunt, når fe₂o₃ -former.
* Du vil lugte svovldioxid (SO₂) gas.
Vigtig note: Den nøjagtige temperatur, hvormed disse reaktioner forekommer, og de dannede specifikke produkter kan variere lidt afhængigt af opvarmningsbetingelserne.
Sidste artikelHvilke hydrofile stoffer er lavet af?
Næste artikelHvilken type kemiker ville beskrive de kemiske egenskaber ilt?
 Varme artikler
Varme artikler
-
 Gør hundefoder mere lækker ved at analysere aromaerKredit:CC0 Public Domain Hunde er ikke kendt for at være kræsne omkring deres mad, spiser den samme kibble dag efter dag med nydelse. Imidlertid, ejere af forkælede pooches vil have, at deres kæle
Gør hundefoder mere lækker ved at analysere aromaerKredit:CC0 Public Domain Hunde er ikke kendt for at være kræsne omkring deres mad, spiser den samme kibble dag efter dag med nydelse. Imidlertid, ejere af forkælede pooches vil have, at deres kæle -
 Højhastigheds FM-AFM og simulering afslører atomistiske opløsningsprocesser af calcit i vand(a) Atomistisk model af calcitoverflade. (b) Opløsningsprocesserne af calcitoverflade i vand observeret med højhastigheds FM-AFM. Det observeres, at trinnet bevæger sig fra nederste højre til øverste
Højhastigheds FM-AFM og simulering afslører atomistiske opløsningsprocesser af calcit i vand(a) Atomistisk model af calcitoverflade. (b) Opløsningsprocesserne af calcitoverflade i vand observeret med højhastigheds FM-AFM. Det observeres, at trinnet bevæger sig fra nederste højre til øverste -
 Hurtige og pålidelige tests for legionellabakterier i vandKredit:Giovanni Cancemi, Shutterstock En fuldautomatisk testanordning kan nu installeres på vandsteder, der er mistænkt for forurening med legionella-bakterier. Enheden lover mere pålidelige resul
Hurtige og pålidelige tests for legionellabakterier i vandKredit:Giovanni Cancemi, Shutterstock En fuldautomatisk testanordning kan nu installeres på vandsteder, der er mistænkt for forurening med legionella-bakterier. Enheden lover mere pålidelige resul -
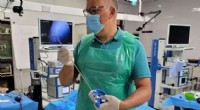 Fremstilling af kirurgiske instrumenter af medicinsk affaldNye styrbare instrumenter til avanceret laparoskopisk kirurgi, delvist lavet af rustfrit stål og blåt polypropylenbetræk, bliver brugt for første gang på Malta. Kredit:Delft University of Technology
Fremstilling af kirurgiske instrumenter af medicinsk affaldNye styrbare instrumenter til avanceret laparoskopisk kirurgi, delvist lavet af rustfrit stål og blåt polypropylenbetræk, bliver brugt for første gang på Malta. Kredit:Delft University of Technology
- Mere afsaltning kommer til Australiens tørreste stater - men supersalt udstrømning kan ødelægge …
- Hvad er 557 newton omregnet i pund?
- Nye DNA -nanoformer tager form
- Måling af nøjagtigheden af livsstilsbaserede domme om politisk tilhørsforhold
- Sådan konverteres negativ Celsius til Fahrenheit
- Hvor vises forstyrrelsen i solen?


