Er frysningspunktet for et blandingsvand og salt højere lavere eller samme rene ingen?
Her er hvorfor:
* frysningspunktdepression: Tilsætning af salt til vand forstyrrer dannelsen af den almindelige iskrystallstruktur. Saltioner (natrium og chlorid) kommer i vejen for vandmolekylerne, der binder sig sammen til et fast stof.
* Kolligativ egenskab: Frysepunktdepression er en colligativ egenskab, hvilket betyder, at det afhænger af antallet af opløste partikler (i dette tilfælde saltioner) opløst i opløsningsmidlet (vand), ikke den specifikke type opløst stof. Jo mere salt du tilføjer, jo lavere frysepunktet.
Dette er grunden til, at salt bruges til at smelte is på veje om vinteren. Salt sænker isens frysepunkt, hvilket får det til at smelte, selv når lufttemperaturen er under 0 ° C (32 ° F).
Sidste artikelHvilken farve drejer salt, når den blandes med flydende indikator?
Næste artikelHvor mange valenselektroner har acetylen?
 Varme artikler
Varme artikler
-
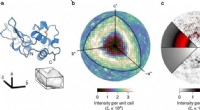 Forskere kortlægger proteinbevægelseret bånddiagram over lysozym (øverst) og den trikliniske enhedscelle, der indeholder et protein (nederst). b Der blev opnået et meget detaljeret tredimensionelt kort over diffus spredning. Den ydre kug
Forskere kortlægger proteinbevægelseret bånddiagram over lysozym (øverst) og den trikliniske enhedscelle, der indeholder et protein (nederst). b Der blev opnået et meget detaljeret tredimensionelt kort over diffus spredning. Den ydre kug -
 Forskere patenterer hurtige tests for kokainFIU biokemi Ph.D. studerende Haixiang Yu, kemi Ph.D. studerende Juan Canoura, og nyuddannet Obtin Alkhamis offentliggjorde en undersøgelse af FIUs patenterede kokaindetektionsteknologier. Kredit:Flori
Forskere patenterer hurtige tests for kokainFIU biokemi Ph.D. studerende Haixiang Yu, kemi Ph.D. studerende Juan Canoura, og nyuddannet Obtin Alkhamis offentliggjorde en undersøgelse af FIUs patenterede kokaindetektionsteknologier. Kredit:Flori -
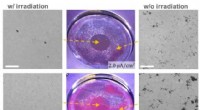 Til ingeniørernes overraskelse, stråling kan bremse korrosion af nogle materialerDisse optiske og scanningselektronmikroskopbilleder viser bestrålede og ubestrålede zoner af en nikkel-chrom legering. Den venstre side viser eksempler på folier med bestråling; i stedet for at forrin
Til ingeniørernes overraskelse, stråling kan bremse korrosion af nogle materialerDisse optiske og scanningselektronmikroskopbilleder viser bestrålede og ubestrålede zoner af en nikkel-chrom legering. Den venstre side viser eksempler på folier med bestråling; i stedet for at forrin -
 Materialeforskere skaber stofalternativer til batterier til bærbare enhederUMass Amherst-forskere ledet af materialekemiker Trisha L. Andrew rapporterer, at de har udviklet en metode til at lave et ladningsopbevarende system, der nemt kan integreres i tøj til at brodere et l
Materialeforskere skaber stofalternativer til batterier til bærbare enhederUMass Amherst-forskere ledet af materialekemiker Trisha L. Andrew rapporterer, at de har udviklet en metode til at lave et ladningsopbevarende system, der nemt kan integreres i tøj til at brodere et l
- Er Apollo 11 Moon Landing Fact eller Fiction?
- Hvilken akvatisk krop er det mest produktive økosystem?
- Redoxdivergerende strategi til konstruktion af (dihydro)thiophener med dimethylsulfoxid
- Fører bekæmpelse af inflation altid til recession? Hvad 60 års NZ-data kan fortælle os
- Hvordan afgiver isotoper energi?
- Hvorfor er radius af en negativ ion altid større end neutralt atom?


