Hvor mange samlede elektroner skal overføres til dannelse af en formelenhed i den sammensatte aluminiumoxat?
1. Identificer ionerne
* Aluminium (AL) danner en +3 ion (al³⁺).
* Oxalat (C₂O₄) danner en -2 ion (C₂O₄²⁻).
2. Bestem formlen
For at afbalancere ladningerne har vi brug for to aluminiumioner (2 x +3 =+6) og tre oxalationer (3 x -2 =-6). Formlen for aluminiumoxalat er al₂ (C₂O₄) ₃ .
3. Beregn elektronoverførsel
* Hvert aluminiumatom mister 3 Elektroner til at blive al³⁺.
* Hver oxalation vinder 2 elektroner til at blive c₂o₄²⁻.
Da vi har to aluminiumioner og tre oxalationer:
* Total elektroner mistet: 2 Alioner * 3 Elektroner/ion =6 elektroner
* Samlede elektroner opnået: 3 c₂o₄²⁻ ioner * 2 elektroner/ion =6 elektroner
Derfor skal i alt 6 elektroner overføres for at danne en formelenhed for aluminiumoxalat.
 Varme artikler
Varme artikler
-
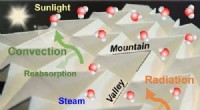 Origami inspirerer til en højeffektiv solar dampgeneratorKredit:American Chemical Society Vand dækker det meste af kloden, men mange regioner lider stadig under mangel på rent drikkevand. Hvis forskerne effektivt og bæredygtigt kunne forvandle havvand t
Origami inspirerer til en højeffektiv solar dampgeneratorKredit:American Chemical Society Vand dækker det meste af kloden, men mange regioner lider stadig under mangel på rent drikkevand. Hvis forskerne effektivt og bæredygtigt kunne forvandle havvand t -
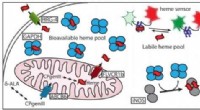 Hvordan celler håndterer en klæbrig, giftig, men absolut essentielt molekyleEt nyligt papir beskriver, hvordan hæm er chaperoneret til dets målproteiner. Kredit:Dennis Stuehr, Cleveland Clinic Nyder du at trække vejret? Du bør spare en tanke en gang imellem for heme, et j
Hvordan celler håndterer en klæbrig, giftig, men absolut essentielt molekyleEt nyligt papir beskriver, hvordan hæm er chaperoneret til dets målproteiner. Kredit:Dennis Stuehr, Cleveland Clinic Nyder du at trække vejret? Du bør spare en tanke en gang imellem for heme, et j -
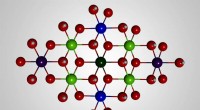 Forskning afslører mekanismen bag en vandspaltningskatalysatorBall-and-stick model af molekylstrukturen af sol-brændstof-katalysatoren udviklet hos Caltech. Blå repræsenterer jernatomer; grøn er nikkel; rød er oxygen; hvid er brint. Kredit:Caltech Caltech-
Forskning afslører mekanismen bag en vandspaltningskatalysatorBall-and-stick model af molekylstrukturen af sol-brændstof-katalysatoren udviklet hos Caltech. Blå repræsenterer jernatomer; grøn er nikkel; rød er oxygen; hvid er brint. Kredit:Caltech Caltech- -
 Brug af en mineralsk svamp til at fange uranEn grafisk illustration af apatit-remedieringstesten for at absorbere uran udført af Sandia, Lawrence Berkeley og Pacific Northwest nationale laboratorier forskere. Kredit:Sandia National Laboratories
Brug af en mineralsk svamp til at fange uranEn grafisk illustration af apatit-remedieringstesten for at absorbere uran udført af Sandia, Lawrence Berkeley og Pacific Northwest nationale laboratorier forskere. Kredit:Sandia National Laboratories
- Et enzym kan reagere med flere underlagskemikalier samtidig?
- Højdepunkt:Nanopatterning af grafen
- Kampen mod antibiotika-resistente bakterier har et glødende nyt våben
- Hvorfor eukaryoter, ikke bakterier, udviklede kompleks multicellularitet
- Effekten af prøvestørrelse på middelværdi & Median
- Undersøgelse analyserer effekten af seksuel orientering på lønninger i Spanien


