Hvad er pH for kobbersulfat?
* ph er et mål for surhed eller alkalinitet af en opløsning. Det bestemmes af koncentrationen af hydrogenioner (H+) i opløsningen.
* kobbersulfat er et salt. Det dannes ved reaktionen af en stærk syre (svovlsyre, H2SO4) og en svag base (kobberhydroxid, Cu (OH) 2).
* PH af en kobbersulfatopløsning afhænger af dens koncentration, og om den er opløst i vand. En opløsning af kobbersulfat i vand vil være let surt på grund af hydrolyse af kobberioner.
Her er en sammenbrud:
* Hydrolyse: Når kobbersulfat opløses i vand, reagerer kobberionerne (Cu²⁺) med vandmolekyler for at danne hydroniumioner (H₃O⁺), som bidrager til surhedsgrad.
* Koncentration: Jo højere koncentration af kobbersulfat er, jo mere sur vil opløsningen være.
For at bestemme den nøjagtige pH for en kobbersulfatopløsning skal du vide:
* Koncentrationen af kobbersulfatopløsningen.
* temperaturen på opløsningen. pH er temperaturafhængig.
Kortfattet: Kobbersulfat i sig selv har ikke en pH. PH af en kobbersulfatopløsning vil være let surt og afhænger af opløsningens koncentration og temperatur.
 Varme artikler
Varme artikler
-
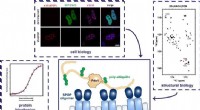 Hvordan ved et reguleringsprotein, hvor det skal bindes for at modulere insulinproduktionen?Penn State -forskere brugte en række forskellige teknikker vedrørende cellebiologi, strukturel biologi, og proteinbiofysik for at bestemme, hvordan proteinerne SPOP og Pdx1 fungerer sammen for at sikr
Hvordan ved et reguleringsprotein, hvor det skal bindes for at modulere insulinproduktionen?Penn State -forskere brugte en række forskellige teknikker vedrørende cellebiologi, strukturel biologi, og proteinbiofysik for at bestemme, hvordan proteinerne SPOP og Pdx1 fungerer sammen for at sikr -
 Kemikere opdager nye signaturer til at identificere cystisk fibrose hos spædbørn førPhilip Britz-McKibbin, Professor i Institut for Kemi og Kemisk Biologi, McMaster University. Kredit:JD Howell, McMaster University Forskere ved McMaster University har opdaget flere nye biomarkøre
Kemikere opdager nye signaturer til at identificere cystisk fibrose hos spædbørn førPhilip Britz-McKibbin, Professor i Institut for Kemi og Kemisk Biologi, McMaster University. Kredit:JD Howell, McMaster University Forskere ved McMaster University har opdaget flere nye biomarkøre -
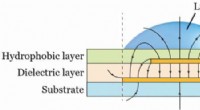 Hydrogel 3-D udskrivning og mønster af væsker med kondensatorkanteffekten (PLEEC)Princippet om PLEEC. En asymmetrisk kondensator er adskilt af et dielektrisk lag. Kredit:Science Advances, doi:10.1126/sciadv.aau8769 Hydrogeler er tredimensionelle (3-D) polymernetværk, der kan t
Hydrogel 3-D udskrivning og mønster af væsker med kondensatorkanteffekten (PLEEC)Princippet om PLEEC. En asymmetrisk kondensator er adskilt af et dielektrisk lag. Kredit:Science Advances, doi:10.1126/sciadv.aau8769 Hydrogeler er tredimensionelle (3-D) polymernetværk, der kan t -
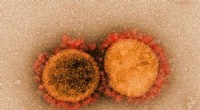 At snyde den nye coronavirus med et falsk håndtrykTransmissionselektronmikrografi af SARS-CoV-2-viruspartikler, isoleret fra en patient. Billede taget og farveforbedret på NIAID Integrated Research Facility (IRF) i Fort Detrick, Maryland. Kredit:NIAI
At snyde den nye coronavirus med et falsk håndtrykTransmissionselektronmikrografi af SARS-CoV-2-viruspartikler, isoleret fra en patient. Billede taget og farveforbedret på NIAID Integrated Research Facility (IRF) i Fort Detrick, Maryland. Kredit:NIAI
- Den indledende massefunktion
- Introduktion til Dead Zone
- Kunne planen for liv være blevet genereret i asteroider?
- Havoverfladetemperaturforskning giver klare beviser for menneskeskabte klimaændringer
- Hvilke to informationsstykker ville du have brug for for at måle masserne stjerner et formørkende …
- Hvad ligner Dalton Model og Electron Cloud Models?


