Hvad er det specielle ved lanthandies og actinider?
1. Position i den periodiske tabel:
* De besætter f-block af den periodiske tabel, der er placeret under hovedkroppen på bordet.
* Denne placering betyder, at deres valenselektroner er i 4f og 5f orbitaler henholdsvis fører til unikke kemiske og fysiske egenskaber.
2. Lignende kemiske egenskaber:
* lanthanides: Disse elementer har meget lignende kemiske egenskaber på grund af afskærmningseffekten af de fyldte 4F -orbitaler. Dette betyder, at de har en tendens til at udvise +3 oxidationstilstande og danne lignende forbindelser.
* actinider: Actinider udviser også lignende kemiske egenskaber, hvor 5F -orbitaler spiller en rolle. De danner ofte komplekse ioner med en række oxidationstilstande.
3. Radioaktiv karakter:
* actinider: Alle actinider er radioaktive, hvor de fleste er meget radioaktive. Dette skyldes ustabiliteten af deres kerner, hvilket resulterer i alfa -forfald og andre radioaktive processer.
4. Diverse applikationer:
* lanthanides: Lanthanides finder adskillige applikationer, herunder:
* fosfor i tv -skærme og fluorescerende lamper
* lasere
* katalysatorer
* magnetiske materialer
* actinider: Actinider, især uran og plutonium , bruges i:
* atomkraftproduktion
* atomvåben
* medicinsk billeddannelse og behandling
5. Elektronisk konfiguration:
* lanthanides: De har en unik elektronisk konfiguration, hvor 4F -orbitaler gradvist fyldes, hvilket fører til en gradvis stigning i atomstørrelse og et fald i ioniseringsenergi over serien.
* actinider: I lighed med lanthanider viser actinider også gradvis fyldning af 5F -orbitaler, men med mere komplekse elektroniske konfigurationer på grund af deres radioaktivitet.
6. Særlige egenskaber:
* paramagnetisme: Både lanthanider og actinider udviser ofte paramagnetisme på grund af tilstedeværelsen af uparrede elektroner i deres F-orbitaler.
* luminescens: Nogle lanthanider er meget selvlysende og udsender lys, når de er begejstrede, hvilket gør dem værdifulde til forskellige applikationer.
* Farve: Mange lanthanid- og actinidforbindelser viser levende farver på grund af f-orbitale overgange, som absorberer og udsender lys i specifikke bølgelængder.
Sammenfattende stammer den specielle karakter af lanthanider og actinider fra deres unikke elektroniske konfigurationer, lignende kemiske egenskaber, radioaktiv karakter, forskellige anvendelser og specielle egenskaber som paramagnetisme og luminescens.
Sidste artikelHvad er et passende opløsningsmiddel til papirkromatografi?
Næste artikelHvad er det samme om isotoper og atom?
 Varme artikler
Varme artikler
-
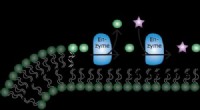 Archaeal enzym, der producerer membranlipider, er spektakulært promiskuøstIllustrationen viser produktionen af forskellige cardiolipiner og fosfolipider ved inkorporering af miljøforbindelser som lipidhovedgruppe. Kredit:Marten Exterkate, Universitetet i Groningen Cel
Archaeal enzym, der producerer membranlipider, er spektakulært promiskuøstIllustrationen viser produktionen af forskellige cardiolipiner og fosfolipider ved inkorporering af miljøforbindelser som lipidhovedgruppe. Kredit:Marten Exterkate, Universitetet i Groningen Cel -
 Molekylær indsigt i edderkoppesilkeSkematisk skema af en spidroin bestående af et samlet C-terminalt domæne (cyan), det udfoldede centrale domæne (hvid linje) og de N-terminale domæner (grøn). Højre side:skema af en tilspidsende spinde
Molekylær indsigt i edderkoppesilkeSkematisk skema af en spidroin bestående af et samlet C-terminalt domæne (cyan), det udfoldede centrale domæne (hvid linje) og de N-terminale domæner (grøn). Højre side:skema af en tilspidsende spinde -
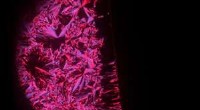 At bryde symmetri fører til responsive organiske fotodetektorerEt polariseret optisk mikroskopibillede af de søjleformede flydende krystaller klemt mellem to krydsede polarisatorer med (højre) og uden (venstre) et elektrisk felt. Dette tyder på, at anvendelse af
At bryde symmetri fører til responsive organiske fotodetektorerEt polariseret optisk mikroskopibillede af de søjleformede flydende krystaller klemt mellem to krydsede polarisatorer med (højre) og uden (venstre) et elektrisk felt. Dette tyder på, at anvendelse af -
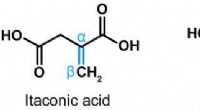 Cellebeskyttelse, immunmodulering og virushæmning af et endogent stofStrukturer af isomererne af itaconsyre. Kredit:CC-BY F. Chen et al. Det endogene molekyle itaconsyre har antivirale og antiinflammatoriske virkninger, som forskere fra TWINCORE for nylig har vist.
Cellebeskyttelse, immunmodulering og virushæmning af et endogent stofStrukturer af isomererne af itaconsyre. Kredit:CC-BY F. Chen et al. Det endogene molekyle itaconsyre har antivirale og antiinflammatoriske virkninger, som forskere fra TWINCORE for nylig har vist.
- Hvordan borer du i granit?
- Forskere dekonstruerer spørgsmål i hjertet af protester, der involverer nationalsang
- NASAs Aqua-satellit ser Tropical Depression 01W ende nær det sydlige Vietnam
- At føle sig ambitiøs, men økonomisk efterladt, brænder på følelsen af utilfredshed med reger…
- Hvornår bliver den første baby født i rummet?
- Jordskælvsekspert, der rådgav Haiti-regeringen i 2010:Hvorfor blev tydelige tidlige advarselsskilt…


