Er organiske forbindelser stabile eller ustabile?
* organiske forbindelser er utroligt forskellige. Der er millioner af forskellige organiske forbindelser, og deres stabilitet varierer meget.
* stabilitet afhænger af det specifikke molekyle. Faktorer som de tilstedeværende bindinger, molekylets struktur og miljøet, det er i al indflydelse på dets stabilitet.
Her er nogle generaliseringer om stabilitet:
* Generelt har organiske forbindelser med stærke, stabile bindinger (som C-C, C-H, C-O) en tendens til at være mere stabile. Disse obligationer er vanskelige at bryde.
* Forbindelser med svage, ustabile bindinger (som c-halogenbindinger) er ofte mere reaktive og mindre stabile. Disse obligationer er lettere at bryde.
* organiske forbindelser kan være ustabile på grund af specifikke funktionelle grupper. For eksempel kan forbindelser med dobbelt- eller tredobbelt bindinger (alkener og alkyner) være mere reaktive end alkaner.
* Miljøet betyder noget. Nogle organiske forbindelser er stabile under normale forhold, men nedbrydes, når de udsættes for varme, lys eller visse kemikalier.
Eksempler:
* methan (CH4) :Meget stabil på grund af dets stærke C-H-obligationer.
* Ethen (C2H4) :Mindre stabil end metan på grund af dens dobbeltbinding, hvilket gør den mere reaktiv.
* acetone (CH3COCH3) :Relativt stabil, men kan nedbrydes under visse betingelser.
Kortfattet:
Det er ikke nøjagtigt at sige, at * alle * organiske forbindelser enten er stabile eller ustabile. Det afhænger af den specifikke forbindelse og de betingelser, den udsættes for. At forstå strukturen og bindingen af organiske molekyler hjælper med at forudsige deres relative stabilitet.
Sidste artikelEr aluminiumsbromid et sammensat element eller en blanding?
Næste artikelHvad er alkaloiders funktion?
 Varme artikler
Varme artikler
-
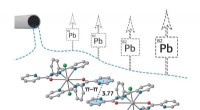 Kemikere foreslår nye reagenser til fjernelse af bly fra spildevandKredit:RUDN University RUDN -universitetets kemikere har sammen med kolleger fra andre lande syntetiseret nye forbindelser, der effektivt binder blyioner og kan bruges til at fjerne det fra spilde
Kemikere foreslår nye reagenser til fjernelse af bly fra spildevandKredit:RUDN University RUDN -universitetets kemikere har sammen med kolleger fra andre lande syntetiseret nye forbindelser, der effektivt binder blyioner og kan bruges til at fjerne det fra spilde -
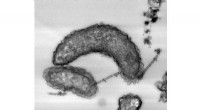 Jernætsende bakterier har vist sig at have enzymer, der gør dem i stand til at udvinde elektroner …Figur:Transmissionselektronmikroskopisk billede af ydre membrancytokromer under elektronkildemangel. Ydre membran (OM) Cytokromer blev farvet på celleoverfladen og nanotråde. Kredit:National Institute
Jernætsende bakterier har vist sig at have enzymer, der gør dem i stand til at udvinde elektroner …Figur:Transmissionselektronmikroskopisk billede af ydre membrancytokromer under elektronkildemangel. Ydre membran (OM) Cytokromer blev farvet på celleoverfladen og nanotråde. Kredit:National Institute -
 Polymer-afledt kulstof som metalfrit, grønt alternativ til katalysatorer og nanocarbonerKredit:CC0 Public Domain Katalysatorer er nøglematerialer i det moderne samfund, muliggør selektiv omdannelse af råvarer til værdifulde produkter, samtidig med at spild reduceres og energi spares.
Polymer-afledt kulstof som metalfrit, grønt alternativ til katalysatorer og nanocarbonerKredit:CC0 Public Domain Katalysatorer er nøglematerialer i det moderne samfund, muliggør selektiv omdannelse af råvarer til værdifulde produkter, samtidig med at spild reduceres og energi spares. -
 Grøn te-molekyle kunne forhindre hjerteanfaldKredit:CC0 Public Domain Grøn te kan være nøglen til at forhindre dødsfald fra hjerteanfald og slagtilfælde forårsaget af åreforkalkning, ifølge forskning finansieret af British Heart Foundation o
Grøn te-molekyle kunne forhindre hjerteanfaldKredit:CC0 Public Domain Grøn te kan være nøglen til at forhindre dødsfald fra hjerteanfald og slagtilfælde forårsaget af åreforkalkning, ifølge forskning finansieret af British Heart Foundation o
- Hvordan teleportering vil fungere
- Single-atom nanozymer
- Er teleportering mulig? Ja, i kvanteverdenen
- Hvilket slutprodukt af Calvin Beson -cyklus bruges til at fremstille glukose og andre sukker?
- CruzAffect:en funktionsrig tilgang til at karakterisere lykke
- Kemikere skaber hurtigere nedbrydende plast til marinebrug


