Hvad er opløseligheden af carbonatsalte?
Her er en sammenbrud:
Faktorer, der påvirker opløselighed:
* kation: Opløseligheden af carbonatsalte er meget afhængig af kationen (den positivt ladede ion).
* gruppe 1 (alkalimetaller) og ammonium (NH4+) carbonater: Disse salte er generelt opløselige i vand.
* gruppe 2 (alkaliske jordmetaller) Carbonater: Disse salte er generelt uopløselige i vand, hvor opløseligheden falder ned i gruppen. For eksempel er calciumcarbonat (CACO3) mindre opløselig end magnesiumcarbonat (MGCO3).
* overgangsmetalcarbonater: Disse salte er generelt uopløselige i vand med nogle undtagelser.
* Temperatur: Opløselighed af carbonatsalte øges generelt med stigende temperatur.
* ph: Opløseligheden af carbonatsalte påvirkes af pH på grund af ligevægtsreaktionerne, der involverer carbonsyre (H2CO3), bicarbonat (HCO3-) og carbonat (CO3^2-) ioner.
Generelle tendenser:
* gruppe 1 og ammoniumcarbonater: Opløselig
* gruppe 2 carbonater: Uopløselig (undtagen BECO3, som er lidt opløselig)
* overgangsmetalcarbonater: Uopløselig (med nogle undtagelser)
Undtagelser:
* beco3: Let opløselig
* srco3: Mere opløselig end caco3
* baco3: Mere opløselig end caco3 og srco3
Vigtig note: Opløselighed er et komplekst fænomen, og den specifikke opløselighed af et carbonatsalt kan påvirkes af forskellige faktorer. Disse generelle tendenser giver et godt udgangspunkt, men det er vigtigt at konsultere pålidelige ressourcer til nøjagtige opløselighedsdata.
Sidste artikelHvad sker der, når overgangsmetaller reagerer med luften?
Næste artikelHvornår nedbryder molekyler næringsstoffer?
 Varme artikler
Varme artikler
-
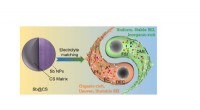 Opnåelse af stabil K-lagringsydelse af carbonkugle-begrænset antimon via elektrolytreguleringDen interne mikrostruktur af Sb@CS med ensartet fordeling af C og Sb udviser helt forskellige egenskaber i to typiske elektrolytter, men den elektrokemiske ydeevne kan opretholde stabilitet efter elek
Opnåelse af stabil K-lagringsydelse af carbonkugle-begrænset antimon via elektrolytreguleringDen interne mikrostruktur af Sb@CS med ensartet fordeling af C og Sb udviser helt forskellige egenskaber i to typiske elektrolytter, men den elektrokemiske ydeevne kan opretholde stabilitet efter elek -
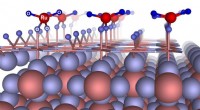 Forskere forklarer pseudocapacitansfænomenet i superkondensatorerKredit:Skoltech Forskere i Rusland og Armenien har forudsagt en ny overfladerekonstruktion af RuO 2 det forklarer oprindelsen af ladningslagring i superkondensatorer. Miniaturiseringen af el
Forskere forklarer pseudocapacitansfænomenet i superkondensatorerKredit:Skoltech Forskere i Rusland og Armenien har forudsagt en ny overfladerekonstruktion af RuO 2 det forklarer oprindelsen af ladningslagring i superkondensatorer. Miniaturiseringen af el -
 Hydrofobe molekylers rolle i katalytiske reaktionerKredit:CC0 Public Domain Elektrokemiske processer kan bruges til at omdanne CO 2 til nyttige udgangsmaterialer til industrien. For at optimere processerne, kemikere forsøger i detaljer at beregn
Hydrofobe molekylers rolle i katalytiske reaktionerKredit:CC0 Public Domain Elektrokemiske processer kan bruges til at omdanne CO 2 til nyttige udgangsmaterialer til industrien. For at optimere processerne, kemikere forsøger i detaljer at beregn -
 Stemplet, espresso, filter? Bare fordi din kaffe er bitter, betyder det ikke, at den er stærkereMoka-gryden, en anden ikonisk italiensk opfindelse, brygger kaffe ved høje temperaturer på en komfur. Kredit:Ccu.bat/Shutterstock Kaffe – en bønne med mange muligheder. Et stort valg er, hvordan ma
Stemplet, espresso, filter? Bare fordi din kaffe er bitter, betyder det ikke, at den er stærkereMoka-gryden, en anden ikonisk italiensk opfindelse, brygger kaffe ved høje temperaturer på en komfur. Kredit:Ccu.bat/Shutterstock Kaffe – en bønne med mange muligheder. Et stort valg er, hvordan ma
- Billede:Multibølgelængdebillede af en supernova-rest
- Hvorfor er areal og hastighed afledte mængder?
- Hvad gør plantecellevægge både stærke og strækbare?
- Hvilken kataklysmisk begivenhed er forbundet med døden af en stjerne?
- Intern kontrol hjælper koraller med at modstå forsuring
- Hvilke grundstoffer er der i ionforbindelser?


