Når forskere ser på carbon-12 og carbon-14, hvad ved de om atomerne?
1. De er isotoper af kulstof: Dette betyder, at de begge har det samme antal protoner (6), men forskellige antal neutroner.
* carbon-12: Har 6 protoner og 6 neutroner. Dette er den mest almindelige og stabile isotop af kulstof.
* carbon-14: Har 6 protoner og 8 neutroner. Dette er en radioaktiv isotop af kulstof.
2. De har forskellige atommasser:
* carbon-12: Har en atommasse på 12 (6 protoner + 6 neutroner)
* carbon-14: Har en atommasse på 14 (6 protoner + 8 neutroner)
3. Carbon-14 er radioaktiv:
* Carbon-14 nedbrydes over tid gennem en proces kaldet beta-forfald, frigiver en beta-partikel (elektron) og omdannes til nitrogen-14.
* Halveringstiden for carbon-14 er 5.730 år, hvilket betyder, at halvdelen af en prøve af carbon-14 vil henfalde til nitrogen-14 i den mængde tid.
4. Carbon-14 kan bruges til radiocarbon-datering:
* På grund af sin radioaktive karakter og kendte halveringstid kan carbon-14 bruges til at datere organiske materialer op til ca. 50.000 år gammel.
* Forskere måler forholdet mellem carbon-14 og carbon-12 i en prøve for at bestemme dens alder.
5. Carbon-12 er standarden for atommasse:
* Carbon-12 bruges som standarden til at definere atommasseenheden (AMU), som er lig med 1/12. massen af et carbon-12-atom.
Ved at studere forskellene mellem carbon-12 og carbon-14 kan forskere få indsigt i:
* Strukturen af atomet: Hvordan antallet af neutroner påvirker atommasse og stabilitet.
* Radioaktivt forfald: Processen med, hvordan ustabile isotoper forvandles til andre elementer.
* Age for gamle materialer: Ved hjælp af carbon-14 datering for at forstå livets historie på jorden.
Sidste artikelHvor mange atomer er der i 68,0 kg?
Næste artikelHvordan kunne Krypton reagere for at opnå en ædel-gas-konfiguration?
 Varme artikler
Varme artikler
-
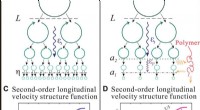 Eksperimentel observation af skalering af det elastiske område i turbulent flow med polymeradditive…Fysisk billede af den turbulente energikaskade og dens manifestation på andenordens longitudinelle hastighedsstrukturfunktion (VSF). (A og B) Tegnefilm, der viser det fysiske billede af energikaskaden
Eksperimentel observation af skalering af det elastiske område i turbulent flow med polymeradditive…Fysisk billede af den turbulente energikaskade og dens manifestation på andenordens longitudinelle hastighedsstrukturfunktion (VSF). (A og B) Tegnefilm, der viser det fysiske billede af energikaskaden -
 Gluten i hvede:Hvad har ændret sig i løbet af 120 års avl?Fra arkivet, forskerne udvalgte fem førende hvedesorter for hvert årti af de undersøgte 120 år. For at generere sammenlignelige prøver, de dyrkede de forskellige sorter i 2015, 2016 og 2017 under samm
Gluten i hvede:Hvad har ændret sig i løbet af 120 års avl?Fra arkivet, forskerne udvalgte fem førende hvedesorter for hvert årti af de undersøgte 120 år. For at generere sammenlignelige prøver, de dyrkede de forskellige sorter i 2015, 2016 og 2017 under samm -
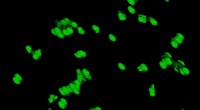 Kostfibre hjælper med at klumpe materiale i din tarmPartikler i tyndtarmsvæsken hos mus ses her i 3D. Musene blev fodret med en standarddiæt. Kredit:Caltech/Ismagilov Lab/A. Preska Steinberg Mad, mikrober, og medicin klumper sig sammen, når de bevæ
Kostfibre hjælper med at klumpe materiale i din tarmPartikler i tyndtarmsvæsken hos mus ses her i 3D. Musene blev fodret med en standarddiæt. Kredit:Caltech/Ismagilov Lab/A. Preska Steinberg Mad, mikrober, og medicin klumper sig sammen, når de bevæ -
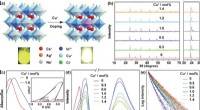 Cu+-doping øger selvfanget exciton-emission i legeret Cs2(Ag/Na)InCl6-dobbeltperovskita) Krystalstruktur af Cs2 (Ag/Na)InCl6 og det krystallografiske sted for Cu+ dopingmidler. PL-fotografierne (λex = 365 nm) for Cs2 (Ag/Na)InCl6 og Cs2 (Ag/Na)InCl6 :1,0 %Cu+ pulvere præsenteres, som v
Cu+-doping øger selvfanget exciton-emission i legeret Cs2(Ag/Na)InCl6-dobbeltperovskita) Krystalstruktur af Cs2 (Ag/Na)InCl6 og det krystallografiske sted for Cu+ dopingmidler. PL-fotografierne (λex = 365 nm) for Cs2 (Ag/Na)InCl6 og Cs2 (Ag/Na)InCl6 :1,0 %Cu+ pulvere præsenteres, som v
- Hvilken enhed vil du bruge til at måle massen af en rosin?
- Hvad er det bedste tidspunkt at se Aurora Borealis?
- Ny samlet teori viser, hvordan tidligere landskaber drev udviklingen af Jordens rige mangfoldighed…
- Hvad er bølgelængden af en rød stjerne?
- Solsystemer kan bruges som ressourcer til planteproduktivitet, undersøgelse viser
- Hvilken har laveste elektronegativitetsjod eller klor?


