Hvad vil det ændre at tilføje en katalysator til kemisk reaktion?
Nøgleeffekter af en katalysator:
* sænket aktiveringsenergi: Katalysatorer giver en alternativ reaktionsvej med en lavere aktiveringsenergi. Dette er den minimale energi, der kræves for reaktanter til at kollidere og danne produkter. Sænkning af aktiveringsenergien betyder, at flere molekyler har nok energi til at reagere, og dermed hurtigere reaktionshastighed.
* øget reaktionshastighed: Da aktiveringsenergien sænkes, kan flere molekyler reagere, hvilket fører til en markant hurtigere reaktionshastighed. Dette er den mest bemærkelsesværdige effekt af en katalysator.
* uændret ligevægtspunkt: Katalysatorer påvirker kun reaktionshastigheden, ikke det endelige ligevægtspunkt. De ændrer ikke mængden af produkter eller reaktanter i ligevægt, hvor hurtigt den ligevægt er nået.
* Selektivitet: Nogle katalysatorer kan selektivt fremme dannelsen af specifikke produkter, der dirigerer reaktionen for at favorisere en bestemt vej.
* ikke konsumeret: Katalysatorer deltager i reaktionsmekanismen, men regenereres i processen. De ændres ikke kemisk eller konsumeres under reaktionen, så de kan deltage i flere reaktionscyklusser.
Eksempler:
* enzymer: Biologiske katalysatorer, der fremskynder biokemiske reaktioner i levende organismer. De er meget specifikke og spiller afgørende roller i alt fra fordøjelse til DNA -replikation.
* katalytiske konvertere: Brugt i biler til at reducere skadelige emissioner ved at katalysere oxidationen af kulilte og kulbrinter til mindre skadeligt kuldioxid og vand.
* Industrielle katalysatorer: Brugt i forskellige brancher til at syntetisere kemikalier, fremstille plast, forfine petroleum og mange andre anvendelser.
Konklusion:
Katalysatorer er kraftfulde værktøjer i kemi, der kan markant fremskynde reaktionerne uden at blive konsumeret sig selv. De sænker aktiveringsenergi, øger reaktionshastighederne og påvirker undertiden produktselektivitet. At forstå katalysatorers rolle er vigtig inden for forskellige områder, fra kemiteknik til biologiske processer.
 Varme artikler
Varme artikler
-
 Smagsligheden mellem fødevarer kan sammenlignes ved hjælp af elektroencefalografiKredit:Pixabay/CC0 Public Domain Marina Domracheva og Sofya Kulikova, forskere fra HSE Universitets campus i Perm, har opdaget en ny tilgang til at analysere den opfattede lighed mellem fødevarer,
Smagsligheden mellem fødevarer kan sammenlignes ved hjælp af elektroencefalografiKredit:Pixabay/CC0 Public Domain Marina Domracheva og Sofya Kulikova, forskere fra HSE Universitets campus i Perm, har opdaget en ny tilgang til at analysere den opfattede lighed mellem fødevarer, -
 RES URBIS-projektet viser levedygtigheden af bioplastproduktion med bioaffald fra byerEn prøve af det brugte affald, det taget produkt fra bakterievirkning, samt flere indhentede bioplastprodukter i projektet. Kredit:J. Mata/UB I en cirkulær økonomi, byaffald bliver omdannet til re
RES URBIS-projektet viser levedygtigheden af bioplastproduktion med bioaffald fra byerEn prøve af det brugte affald, det taget produkt fra bakterievirkning, samt flere indhentede bioplastprodukter i projektet. Kredit:J. Mata/UB I en cirkulær økonomi, byaffald bliver omdannet til re -
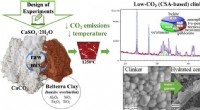 Alternativ cement med lavt CO2-fodaftryk udvikletGrafisk abstrakt. Kredit:DOI:10.1016/j.susmat.2021.e00299 Forskere ved Martin Luther University Halle-Wittenberg (MLU) i Tyskland og det brasilianske universitet i Pará har udviklet et klimavenlig
Alternativ cement med lavt CO2-fodaftryk udvikletGrafisk abstrakt. Kredit:DOI:10.1016/j.susmat.2021.e00299 Forskere ved Martin Luther University Halle-Wittenberg (MLU) i Tyskland og det brasilianske universitet i Pará har udviklet et klimavenlig -
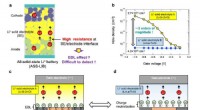 Ny måde at undersøge den elektriske dobbeltlagseffekt på(a) Diagram over et hel-solid-state Li-ion batteri, der lider af høj grænseflademodstand, formodes at skyldes EDL-effekten. (b) Diamantbaserede felteffekttransistorer (FETer) lader os modulere huldens
Ny måde at undersøge den elektriske dobbeltlagseffekt på(a) Diagram over et hel-solid-state Li-ion batteri, der lider af høj grænseflademodstand, formodes at skyldes EDL-effekten. (b) Diamantbaserede felteffekttransistorer (FETer) lader os modulere huldens
- Hvad er industriel smog?
- Hvordan arbejdere bliver forført af dyrkelsen af optimal travlhed
- Molekyler, der har en ulig fordeling af ladninger?
- Nye data viser, at amerikanske hadforbrydelser fortsatte med at stige i 2017
- Bullfinker holder sammen i årevis
- Hvad er en gruppe af løse klipper, der falder eller ruller ned ad stejl hældning?


