Hvad påvirker sammensætningen af et vand dets ladning?
* vandmolekyler (H₂O) er polære: Oxygenatomet i et vandmolekyle er lidt negativt ladet, mens brintatomerne er lidt positivt ladet. Dette skaber et dipolmoment, hvor den ene ende af molekylet er lidt positivt og den anden lidt negativ.
* ioniske bindinger: Når vand opløses salte eller andre ioniske forbindelser, adskiller de positive og negative ioner sig. De positive ioner tiltrækkes af den negative ende af vandmolekyler, mens de negative ioner tiltrækkes af den positive ende. Denne proces kaldes hydrering.
* ligevægt: Selv i rent vand er der en lille mængde ionisering, hvor vandmolekyler bryder fra hinanden i H+ (hydrogen) og OH- (hydroxid) ioner. Imidlertid findes disse ioner i lige store mængder og opretholder en neutral samlet ladning.
Hvad kan ændre sigt for vandet?
* opløste ioner: Hvis du opløser mere positive ioner (som natriumioner fra bordsalt) end negative ioner, vil vandopløsningen have en netto -positiv ladning. Det modsatte er sandt, hvis du opløser flere negative ioner (som chloridioner).
* ph: PH af en opløsning er et mål for dens hydrogenion (H+) koncentration. En lav pH (sur) betyder, at der er flere H+ -ioner, hvilket giver løsningen en positiv ladning. En høj pH (alkalisk/basisk) betyder, at der er flere ohioner, hvilket giver løsningen en negativ ladning.
Key Takeaway: Mens rent vand er neutralt, kan tilstedeværelsen af opløste ioner og ændringer i pH påvirke den samlede ladning af en vandopløsning.
Sidste artikelHvad er alkalimetaller?
Næste artikelHvad er elektronkonfigurationen af AL?
 Varme artikler
Varme artikler
-
 Ny overfladebehandling kan forbedre køleeffektivitetenEn glat overflade til væsker med meget lav overfladespænding fremmer dråbedannelse, lette varmeoverførslen. Kredit:Karim Khalil et al . I modsætning til vand, flydende kølemidler og andre væsk
Ny overfladebehandling kan forbedre køleeffektivitetenEn glat overflade til væsker med meget lav overfladespænding fremmer dråbedannelse, lette varmeoverførslen. Kredit:Karim Khalil et al . I modsætning til vand, flydende kølemidler og andre væsk -
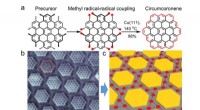 Syntese på overfladen af grafenmolekyler og deres supergitterFigur viser transformationen fra precursor-molekylet til det atomisk præcise circumcoronen-supergitter. (a) Precursormolekylet gennemgår en kemisk cyclodehydrogeneringsproces med brug af kobber (111)
Syntese på overfladen af grafenmolekyler og deres supergitterFigur viser transformationen fra precursor-molekylet til det atomisk præcise circumcoronen-supergitter. (a) Precursormolekylet gennemgår en kemisk cyclodehydrogeneringsproces med brug af kobber (111) -
 Kemikere finder nye måder at skabe byggestenene i mange lægemidler påZuxiao Zhang i Nagib-laboratoriet ved Ohio State University. Zhang og andre organiske kemikere har fundet ud af, hvordan man skaber et syntetisk molekyle, der er en afgørende byggesten til fremstillin
Kemikere finder nye måder at skabe byggestenene i mange lægemidler påZuxiao Zhang i Nagib-laboratoriet ved Ohio State University. Zhang og andre organiske kemikere har fundet ud af, hvordan man skaber et syntetisk molekyle, der er en afgørende byggesten til fremstillin -
 Studer polyfarmakologi tidligere i lægemiddelopdagelsen, siger forskereKredit:CC0 Public Domain Polyfarmakologi - et lægemiddels evne til at påvirke mere end ét protein - bør studeres tidligt i lægemiddelopdagelsesforløbet, og konstant overvåget, da den kemiske struk
Studer polyfarmakologi tidligere i lægemiddelopdagelsen, siger forskereKredit:CC0 Public Domain Polyfarmakologi - et lægemiddels evne til at påvirke mere end ét protein - bør studeres tidligt i lægemiddelopdagelsesforløbet, og konstant overvåget, da den kemiske struk
- NASAs Webb-cam fanger ingeniører på arbejde på Webb i Johnson Space Center
- Nanopartikelskærm kunne fremskynde udviklingen af lægemidler
- Simuleringer viser, hvordan beta-amyloid kan dræbe neurale celler
- Hvilken type videnskabsmand studerer biotiske faktorer?
- Aldersdata viser, at planetesimaler leverede byggematerialer til vandrige planeter i det tidlige sol…
- Kan jeg se Uranus med det blotte øje fra Jorden"?


