Hvad er bærere af strøm i en elektrolytisk opløsning?
Her er en sammenbrud:
* Elektrolytisk opløsning: Dette er en opløsning, der indeholder opløste ioner, dannet, når en ionisk forbindelse opløses i et opløsningsmiddel (normalt vand).
* ioner: Dette er atomer eller molekyler, der har vundet eller mistet elektroner, hvilket giver dem en nettopositiv eller negativ ladning.
* strømstrøm: I en elektrolytisk opløsning bæres strøm af bevægelsen af disse ladede ioner.
* kationer (positivt ladede ioner): De bevæger sig mod den negative elektrode (katode).
* anioner (negativt ladede ioner): De bevæger sig mod den positive elektrode (anode).
Eksempel: I en opløsning af NaCl (tabel salt) føres strømmen af bevægelsen af natriumioner (Na+) og chloridioner (Cl-).
nøglepunkter at huske:
* I modsætning til i metaller, hvor elektroner er de nuværende bærere, i elektrolytiske opløsninger, er det bevægelsen af ladede ioner, der udgør strømmen af strøm.
* Konduktiviteten af en elektrolytisk opløsning afhænger af koncentrationen af ioner, der er til stede. Højere ionkoncentration fører til højere ledningsevne.
 Varme artikler
Varme artikler
-
 Biosensor muliggør iltovervågning i realtid for organer-på-en-chipEn ny biosensor giver forskere mulighed for at spore iltniveauer i realtid i organ-on-a-chip-systemer, gør det muligt at sikre, at sådanne systemer i højere grad efterligner virkelige organers funktio
Biosensor muliggør iltovervågning i realtid for organer-på-en-chipEn ny biosensor giver forskere mulighed for at spore iltniveauer i realtid i organ-on-a-chip-systemer, gør det muligt at sikre, at sådanne systemer i højere grad efterligner virkelige organers funktio -
 Hvordan deformeres blodlegemer, komme sig, når man rejser gennem små kanalerRøde blodlegemer genopretter deres form på to måder efter at have strømmet gennem trange kanaler. Kredit:A. Amirouche, Université Lyon Laboratorieblodprøver udføres ofte ved at tvinge prøver genne
Hvordan deformeres blodlegemer, komme sig, når man rejser gennem små kanalerRøde blodlegemer genopretter deres form på to måder efter at have strømmet gennem trange kanaler. Kredit:A. Amirouche, Université Lyon Laboratorieblodprøver udføres ofte ved at tvinge prøver genne -
 Katalysator muliggør reaktioner ved hjælp af grønt lysKolber indeholdende titaniumkatalysatoren og det røde farvestof, som bestråles med grønt lys i laboratoriet på Kekulé Institute of Organic Chemistry and Biochemistry ved universitetet i Bonn. Kredit:Z
Katalysator muliggør reaktioner ved hjælp af grønt lysKolber indeholdende titaniumkatalysatoren og det røde farvestof, som bestråles med grønt lys i laboratoriet på Kekulé Institute of Organic Chemistry and Biochemistry ved universitetet i Bonn. Kredit:Z -
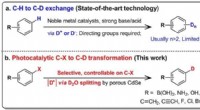 Præcis deuteration ved hjælp af tungt vandFigur viser sammenligningen mellem den konventionelle H/D-udveksling (baseret på CH-bindinger) og den nye tungvandssplittemetode (baseret på C-X-bindinger). Kredit:National University of Singapore
Præcis deuteration ved hjælp af tungt vandFigur viser sammenligningen mellem den konventionelle H/D-udveksling (baseret på CH-bindinger) og den nye tungvandssplittemetode (baseret på C-X-bindinger). Kredit:National University of Singapore
- Kan du se Mars fra Jupiter?
- Undersøgelse finder sammenhænge mellem skovrydning og fiskeriudbytter i Amazonas
- Hvad er de 5 hårdeste klipper i verden?
- Bøjbart batteri og LED udgør det første funktionelle helt fleksible elektroniske system
- Dette er en simpel maskine, der består af et skråplan viklet rundt om midterstolpen.?
- Hvad skete der med natriumchloridkrystallerne, når der blev tilsat 5 ml vand?


