Hvilke forbindelser har aluminium på det periodiske tabel?
Almindelige aluminiumsforbindelser:
* aluminiumoxid (al₂o₃): Dette er en meget almindelig forbindelse, der naturligt findes som mineralkorund. Det bruges i keramik, slibemidler og endda som base for ædelsten som Ruby og Sapphire.
* aluminium hydroxid (AL (OH) ₃): Brugt i antacida, vandbehandling og som en komponent af nogle brandhæmmere.
* aluminiumchlorid (alcl₃): Bruges som katalysator i kemiske reaktioner og som en komponent af nogle deodoranter.
* aluminiumssulfat (al₂ (so₄) ₃): Brugt i papirfremstilling, vandbehandling og som en koagulant i forskellige processer.
* aluminiumnitrat (AL (no₃) ₃): Bruges i eksplosiver, som en mordant i farvning og i nogle ildslukkere.
* aluminiumphosphat (alpo₄): Fundet i nogle gødninger og brugt i tandcement.
Bemærk: Dette er bare nogle eksempler. Aluminium danner en lang række forbindelser på grund af dens evne til at miste tre elektroner og danne en +3 -kation.
Husk:Aluminium i sig selv er et element, ikke en forbindelse. Disse er forbindelser * indeholdende * aluminium.
Sidste artikelHvorfor er lanthaniderne og sctiniderne placeret i bunden af periodisk bord?
Næste artikelHvad er de typer giftige gasser?
 Varme artikler
Varme artikler
-
 En god defekt? Forskere opdager spiralformede skrueforskydninger i lagdelte polymererEn helicoid struktur har to sider (overflader). Hvis den ene side er materiale A, og den anden side er materiale B, er det muligt at tværgående uafbrudt langs defekten, der bliver inden for A-laget ud
En god defekt? Forskere opdager spiralformede skrueforskydninger i lagdelte polymererEn helicoid struktur har to sider (overflader). Hvis den ene side er materiale A, og den anden side er materiale B, er det muligt at tværgående uafbrudt langs defekten, der bliver inden for A-laget ud -
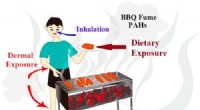 Hud ansvarlig for større eksponering for kræftfremkaldende stoffer i grillrøg end lungerKredit:American Chemical Society Med sommeren på vej, det er kun et spørgsmål om tid, før duften og smagen af grillmad dominerer nabolaget. Men der er en ulempe ved at grille, som bogstaveligt t
Hud ansvarlig for større eksponering for kræftfremkaldende stoffer i grillrøg end lungerKredit:American Chemical Society Med sommeren på vej, det er kun et spørgsmål om tid, før duften og smagen af grillmad dominerer nabolaget. Men der er en ulempe ved at grille, som bogstaveligt t -
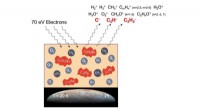 Lifes byggesten observeret i rumlignende omgivelserLavenergi-elektronpåvirkning formidler skabelsen af nye komplekse organiske molekyler, såsom ethanol, i astrofysiske/planetariske modelis indeholdende metan og ilt; mens nogle af de nye arter desorb
Lifes byggesten observeret i rumlignende omgivelserLavenergi-elektronpåvirkning formidler skabelsen af nye komplekse organiske molekyler, såsom ethanol, i astrofysiske/planetariske modelis indeholdende metan og ilt; mens nogle af de nye arter desorb -
 Bygning af stilladser ved hjælp af eksotiske elementer:Forskerhold lykkes med at skabe nye metal-or…Dr. Juliane März ved handskerummet. Her forbereder hun en fugt- og iltfølsom prøve til analyse. Kredit:Amac Garbe/HZDR Efter deres opdagelse for 25 år siden, fik metal-organiske rammer (MOFer) hurt
Bygning af stilladser ved hjælp af eksotiske elementer:Forskerhold lykkes med at skabe nye metal-or…Dr. Juliane März ved handskerummet. Her forbereder hun en fugt- og iltfølsom prøve til analyse. Kredit:Amac Garbe/HZDR Efter deres opdagelse for 25 år siden, fik metal-organiske rammer (MOFer) hurt
- Store lastbiler er de største skyldige i luftforurening nær vej
- Hvad er det tryk, der udøves af en væske total kraft, der er skillet af?
- Kina forsinker lanceringen for at færdiggøre GPS-lignende Beidou-netværk
- Hjælper gadesexarbejdere med at bryde cyklussen af hjemløshed
- Ny undersøgelse afslører mysteriet med henfaldende exoplanetbaner
- Er Californien blackouts det nye normale for staten?


