Hvorfor er lanthaniderne og sctiniderne placeret i bunden af periodisk bord?
1. Rumbegrænsninger:
* Den periodiske tabel er organiseret ved at øge atomnummeret og elektronkonfiguration.
* Lanthaniderne og actiniderne har meget ens kemiske egenskaber på grund af deres F-blok-elektronkonfiguration.
* Inklusive dem i hovedkroppen på bordet ville gøre det for bredt og uhåndterligt og forstyrre den visuelle organisation.
2. Opretholdelse af periodicitet:
* Placering af dem i bunden gør det muligt for hovedkroppen at afspejle elementernes periodicitet med hensyn til deres kemiske egenskaber og valenselektronkonfigurationer.
* Dette arrangement holder elementer med lignende kemiske egenskaber i de samme lodrette søjler (grupper).
3. Visuel klarhed:
* Dette arrangement understreger Lanthanides og Actinides unikke karakter som separate serier med forskellige egenskaber.
4. Historiske grunde:
* Tidlige versioner af den periodiske tabel inkluderede ikke disse elementer.
* Da de blev opdaget, fremkom placeringen i bunden som den mest logiske løsning for at opretholde tabellens struktur og organisering.
Kortfattet: At placere lanthaniderne og actiniderne i bunden af den periodiske tabel er en praktisk og logisk løsning, der:
* Bevarer organiseringen af tabellen baseret på elektronkonfiguration.
* Opretholder de periodiske tendenser for kemiske egenskaber.
* Giver visuel klarhed.
* Reflekterer historisk udvikling af tabellen.
Sidste artikelHvor mange atomer udgør elementet CUS04?
Næste artikelHvilke forbindelser har aluminium på det periodiske tabel?
 Varme artikler
Varme artikler
-
 Ny 3D-printteknik er en game changer for medicinske testenhederEt eksempel på en mikrofluidisk chip skabt af forskerholdet. Kredit:Yang Xu Mikrofluidiske enheder er kompakte testværktøjer, der består af bittesmå kanaler skåret på en chip, som gør det muligt fo
Ny 3D-printteknik er en game changer for medicinske testenhederEt eksempel på en mikrofluidisk chip skabt af forskerholdet. Kredit:Yang Xu Mikrofluidiske enheder er kompakte testværktøjer, der består af bittesmå kanaler skåret på en chip, som gør det muligt fo -
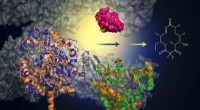 Forskere udvikler grønnere og mere effektiv metode til fremstilling af næste generations antibioti…Med tilføjelsen af en murin-afledt biokatalysator (grøn), kan dette konstruerede protein tilføje et fluoridatom for at skabe makrolidanaloger (struktur, til højre). Denne tilgang tilbyder en grønner
Forskere udvikler grønnere og mere effektiv metode til fremstilling af næste generations antibioti…Med tilføjelsen af en murin-afledt biokatalysator (grøn), kan dette konstruerede protein tilføje et fluoridatom for at skabe makrolidanaloger (struktur, til højre). Denne tilgang tilbyder en grønner -
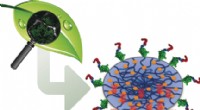 Mikroleveringsservice for gødningKredit:Wiley Planter kan optage næringsstoffer gennem deres blade såvel som deres rødder. Imidlertid, bladgødskning over en længere periode er vanskelig. I journalen Angewandte Chemie , Tyske fo
Mikroleveringsservice for gødningKredit:Wiley Planter kan optage næringsstoffer gennem deres blade såvel som deres rødder. Imidlertid, bladgødskning over en længere periode er vanskelig. I journalen Angewandte Chemie , Tyske fo -
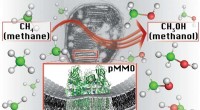 Metanforbrugende bakterier kan være fremtiden for brændstofDet primære metaboliske enzym i metanotrofe bakterier, partikelformig methanmonooxygenase (pMMO), katalyserer metan-til-methanol-omdannelsen på et sted med en kobberion. Kredit:Northwestern University
Metanforbrugende bakterier kan være fremtiden for brændstofDet primære metaboliske enzym i metanotrofe bakterier, partikelformig methanmonooxygenase (pMMO), katalyserer metan-til-methanol-omdannelsen på et sted med en kobberion. Kredit:Northwestern University
- Hvem opdagede Saturn -måner?
- Træning hjælper lærere med at forudse, hvordan elever med indlæringsvanskeligheder kan løse pro…
- Hvordan laver man klæbemidler til elektronik, køretøjer, og konstruktion hårdere?
- Hvorfor har siliciumtetrachlorid lavt smeltepunkt?
- Luftforurening fra olie- og gasproduktionssteder synlig fra rummet
- Modellen forudser, at lithium-ion-batterier er mest konkurrencedygtige til opbevaringsapplikationer …


