Mol gasser ved standardtemperaturtryk?
Dette er kendt som molvolumen af en ideel gas ved STP .
Det er vigtigt at bemærke, at:
* Denne værdi er kun gyldig for ideelle gasser . Ægte gasser kan afvige lidt fra denne værdi på grund af intermolekylære kræfter og andre faktorer.
* Definitionen af STP har udviklet sig over tid. Nogle kilder kan bruge lidt forskellige definitioner til STP, som kan påvirke det molære volumen.
Her er en sammenbrud:
* mol: En måleenhed, der repræsenterer en bestemt mængde stof. En mol indeholder Avogadros antal partikler (6,022 x 10^23).
* standardtemperatur og tryk (STP): Et sæt standardbetingelser, der bruges til sammenligning af gasegenskaber.
* molvolumen: Volumenet besat af en mol af et stof.
Derfor, hvis du kender mængden af en gas ved STP, kan du beregne antallet af mol ved hjælp af følgende formel:
Antal mol =volumen gas (L)/molvolumen (L/mol)
For eksempel, hvis en gas besætter 44,8 liter på STP, ville antallet af mol være:
Antal mol =44,8 L/22,4 L/mol =2 mol
Sidste artikelHvad er forholdet mellem gastemperatur og volumen?
Næste artikelEr evnen til at rustne en kemisk egenskab?
 Varme artikler
Varme artikler
-
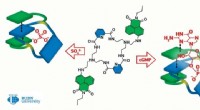 Kemikere skaber et molekyle, der kan hjælpe med at behandle hjertesygdomme og opdage viraKredit:RUDN Universitet RUDN University kemikere sammen med kolleger fra Chemnitz University of Technology (Tyskland) har syntetiseret den første kemiske receptor, der effektivt kan binde til cykl
Kemikere skaber et molekyle, der kan hjælpe med at behandle hjertesygdomme og opdage viraKredit:RUDN Universitet RUDN University kemikere sammen med kolleger fra Chemnitz University of Technology (Tyskland) har syntetiseret den første kemiske receptor, der effektivt kan binde til cykl -
 Forskere skaber nyt materiale til fremtidens elektronikLeder af Laboratoriet for Krystalvækst, Professor, Ph.D. Denis Vinnik Kredit:SUSU Forskere ved South Ural State University er ved at skabe et nyt materiale med foruddefinerede egenskaber. Det vil
Forskere skaber nyt materiale til fremtidens elektronikLeder af Laboratoriet for Krystalvækst, Professor, Ph.D. Denis Vinnik Kredit:SUSU Forskere ved South Ural State University er ved at skabe et nyt materiale med foruddefinerede egenskaber. Det vil -
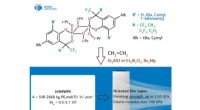 En undersøgelse af katalysatorer til syntetisering af polyethylen med ultrahøj molekylvægtKredit:RUDN Universitet En kemiker fra RUDN University som en del af et team af forskere har syntetiseret nye højaktive katalysatorer til fremstilling af polyethylen med ultrahøj molekylvægt, som
En undersøgelse af katalysatorer til syntetisering af polyethylen med ultrahøj molekylvægtKredit:RUDN Universitet En kemiker fra RUDN University som en del af et team af forskere har syntetiseret nye højaktive katalysatorer til fremstilling af polyethylen med ultrahøj molekylvægt, som -
 Kontrol af kunstige cilia med magnetfelter og lysFotografi af en række magnetiske cilia foldet og holdt i spidsen af pincet. Kredit:Jessica A.-C. Liu Forskere fra North Carolina State University og Elon University har lavet kunstige cilia, ell
Kontrol af kunstige cilia med magnetfelter og lysFotografi af en række magnetiske cilia foldet og holdt i spidsen af pincet. Kredit:Jessica A.-C. Liu Forskere fra North Carolina State University og Elon University har lavet kunstige cilia, ell


