Hvordan ændrede resultaterne af JJ -eksperimenter, hvordan forskere tænkte over atomer?
før Thomsons eksperimenter:
* Daltons atomteori: Før Thomson var den herskende model af atomet John Daltons teori. Denne teori foreslog, at atomer var udelelige, solide sfærer.
* Ingen viden om subatomære partikler: Forskere havde ikke noget begreb om mindre partikler inden for atomet, som elektroner, protoner eller neutroner.
Thomsons eksperimenter og deres indflydelse:
* Opdagelse af elektronet: Thomsons eksperimenter demonstrerede eksistensen af negativt ladede partikler, som han kaldte elektroner. Dette var et stort gennembrud, hvilket beviser, at atomer ikke var udelelige.
* blomme budding model: Baseret på hans eksperimenter foreslog Thomson atomets "blomme budding". Denne model så for sig atomet som en sfære af positivt ladet materiale med negativt ladede elektroner indlejret i det som blommer i en budding.
* atom er ikke solidt: Thomsons arbejde viste, at atomer havde en intern struktur og ikke blot var solide sfærer. Dette udfordrede den tidligere forståelse af atomet.
Konsekvenser af den nye forståelse:
* atom som et komplekst system: Opdagelsen af elektronet åbnede døren til en mere kompleks overblik over atomet. Forskere begyndte at undersøge muligheden for andre subatomære partikler, og hvordan de interagerede.
* Foundation for fremtidige opdagelser: Thomsons arbejde banede vejen for senere eksperimenter som Rutherfords guldfolieeksperiment, hvilket førte til udviklingen af atomets nukleare model.
Kortfattet:
J.J. Thomsons eksperimenter ændrede grundlæggende vores forståelse af atomet. Han beviste, at atomer ikke var udelelige og havde intern struktur. Denne opdagelse førte til udviklingen af nye atommodeller og ansporet yderligere forskning i stofets grundlæggende karakter.
Sidste artikelHvad er forskellen mellem kemisk forandring og fysisk forandring?
Næste artikelHvad består hvid eddike af?
 Varme artikler
Varme artikler
-
 Forskning nulstilling på elektronisk næse til overvågning af luftkvalitet, diagnosticering af syg…Afbildning af et gassensorarray sammensat af mikroskalabalancer belagt med tynde film af nanoporøse materialer kaldet metalorganiske rammer. Kredit:Arni Sturluson, Melanie Huynh, OSU Ingeniørhøjskole
Forskning nulstilling på elektronisk næse til overvågning af luftkvalitet, diagnosticering af syg…Afbildning af et gassensorarray sammensat af mikroskalabalancer belagt med tynde film af nanoporøse materialer kaldet metalorganiske rammer. Kredit:Arni Sturluson, Melanie Huynh, OSU Ingeniørhøjskole -
 Fremskridt inden for cellulosebaseret fødevareemballage går videre til testfasen af industriel p…Kredit:Pixabay/CC0 Public Domain VTT tester Thermocell -plastfilm fremstillet af cellulose og fedtsyrer i produktionen af mademballage i samarbejde med Arla Foods, Paulig, og Wipak. Termocelle p
Fremskridt inden for cellulosebaseret fødevareemballage går videre til testfasen af industriel p…Kredit:Pixabay/CC0 Public Domain VTT tester Thermocell -plastfilm fremstillet af cellulose og fedtsyrer i produktionen af mademballage i samarbejde med Arla Foods, Paulig, og Wipak. Termocelle p -
 Bakterieudvikling markerer en ny æra inden for cellulært designGrafisk billede af rørformede stilladser i celler. Kredit:University of Kent Forskere ved universiteterne i Kent og Bristol har bygget et miniaturestillads inde i bakterier, der kan bruges til at
Bakterieudvikling markerer en ny æra inden for cellulært designGrafisk billede af rørformede stilladser i celler. Kredit:University of Kent Forskere ved universiteterne i Kent og Bristol har bygget et miniaturestillads inde i bakterier, der kan bruges til at -
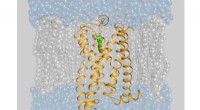 Farmakonutrition:Moderne lægemiddeldesign til funktionelle undersøgelserModel af den bitre receptor TAS2R14 med en af dens aktivatorer (ligander), flufenaminsyren. Kredit:Antonella Di Pizio/Leibniz-LSB@TUM Antonella Di Pizio og Maik Behrens fra Leibniz-instituttet f
Farmakonutrition:Moderne lægemiddeldesign til funktionelle undersøgelserModel af den bitre receptor TAS2R14 med en af dens aktivatorer (ligander), flufenaminsyren. Kredit:Antonella Di Pizio/Leibniz-LSB@TUM Antonella Di Pizio og Maik Behrens fra Leibniz-instituttet f
- Hvilke to former kommer prokaryoter ind?
- Forskere øger følsomheden og hastigheden af Raman-mikroskopiteknikken
- Lanthan chromoxider energisk dans med lys
- Facebook-rapport viser tilhængere af amerikanske politiske annoncer
- Hvorfor smelter salt is hurtigere end sukker?
- Hvorfor er atomer af metaller og ikke reaktive?


