Hvilke egenskaber ved salt?
egenskaber ved salt (natriumchlorid)
Salt (NaCl) er en almindelig og væsentlig forbindelse med adskillige egenskaber, både fysisk og kemisk:
Fysiske egenskaber:
* udseende: Hvid, krystallinsk fast stof.
* smag: Saltet.
* lugt: Lugtfri.
* opløselighed: Meget opløselig i vand og danner en klar opløsning.
* smeltepunkt: 801 ° C (1474 ° F)
* kogepunkt: 1413 ° C (2575 ° F)
* densitet: 2,16 g/cm³
* hårdhed: Relativt blød, let ridset.
* Krystallinsk struktur: Kubik (NaCl krystalliserer i en ansigt-centreret kubisk gitterstruktur).
* Konduktivitet: Ikke-ledende i fast form, men ledende, når det blev opløst i vand.
Kemiske egenskaber:
* ionisk forbindelse: Sammensat af positivt ladede natriumioner (Na+) og negativt ladede chloridioner (Cl-).
* elektrolyt: Når det er opløst i vand, adskiller den sig til ioner, hvilket gør opløsningen elektrisk ledende.
* stabil: Kemisk stabil under normale forhold.
* Hygroskopisk: Kan absorbere fugt fra luften og blive lidt fugtig.
* reagerer med syrer: Reagerer med syrer til dannelse af salte og saltsyre (HCI).
* reagerer med baser: Reagerer med baser til dannelse af salte og natriumhydroxid (NaOH).
Andre egenskaber:
* konserveringsmiddel: Salt er blevet brugt som konserveringsmiddel til mad i århundreder, da det hæmmer mikrobiel vækst.
* smagsforstærker: Salt forbedrer smagen af mad.
* essentiel næringsstof: Natrium og chlorid er vigtige mineraler, der kræves til menneskers sundhed.
* smeltning og frysepunktdepression: Salt kan sænke det frysepunkt for vand, hvilket gør det nyttigt ved at afseveje og fortove.
* Brugt i forskellige brancher: Salt bruges i en lang række industrier, herunder kemikalier, fødevareforarbejdning, farmaceutiske stoffer og vandbehandling.
Vigtig note: Mens salt er vigtigt, kan det at forbruge for meget være skadeligt for helbredet. Den anbefalede daglige indtag varierer afhængigt af individuelle behov og bør diskuteres med en sundhedspersonale.
Sidste artikelHvad ville der ske, hvis materialer ikke forfaldt?
Næste artikelHvorfor mineralolie opløses i hexan og ikke vand?
 Varme artikler
Varme artikler
-
 Forskere opdager ny kemisk reaktionKredit:CC0 Public Domain At finde noget så nyt, at det kan indgå i lærebøger som grundlæggende viden er enhver videnskabsmands drøm, siger prof. dr. Jan Paradies, professor ved Paderborn Universite
Forskere opdager ny kemisk reaktionKredit:CC0 Public Domain At finde noget så nyt, at det kan indgå i lærebøger som grundlæggende viden er enhver videnskabsmands drøm, siger prof. dr. Jan Paradies, professor ved Paderborn Universite -
 Cyanobakterier som grønne katalysatorer i bioteknologiCyanobakterier er miljøvenlige og let tilgængelige biokatalysatorer til produktion af nye kemikalier og, takket være forskere ved TU Graz, snart kunne bruges i store teknologiske applikationer. Kredit
Cyanobakterier som grønne katalysatorer i bioteknologiCyanobakterier er miljøvenlige og let tilgængelige biokatalysatorer til produktion af nye kemikalier og, takket være forskere ved TU Graz, snart kunne bruges i store teknologiske applikationer. Kredit -
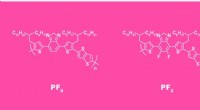 Forskere opgraderer organiske solceller til brug i tagsten, der producerer strømStrukturen af en gentagende enhed i polymerkæden uden fluor (venstre) og efter fluorering (højre). Kredit:Elena Khavina/MIPT Et internationalt team af materialeforskere fra Frankrig, Rusland og
Forskere opgraderer organiske solceller til brug i tagsten, der producerer strømStrukturen af en gentagende enhed i polymerkæden uden fluor (venstre) og efter fluorering (højre). Kredit:Elena Khavina/MIPT Et internationalt team af materialeforskere fra Frankrig, Rusland og -
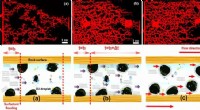 En ny klasse af forgrenede enkeltkædede overfladeaktive stoffer til forbedret olieudvinding rapport…Øverst:Forskelle i bevægelsen af olie gennem mikrokanalerne efter opløsningens oversvømmelse af (a) ren saltlage, b) rent overfladeaktivt stof og (c) overfladeaktivt middel-saltvand. Nederst:Skemati
En ny klasse af forgrenede enkeltkædede overfladeaktive stoffer til forbedret olieudvinding rapport…Øverst:Forskelle i bevægelsen af olie gennem mikrokanalerne efter opløsningens oversvømmelse af (a) ren saltlage, b) rent overfladeaktivt stof og (c) overfladeaktivt middel-saltvand. Nederst:Skemati
- Forfølger dronerne
- Amerikanerne er ikke økonomisk forberedt på alderdommen, undersøgelse finder
- Indfødte i Alaska og fiskere sagsøger EPA for at omgøre Pebble Mine-beslutningen
- Hvad sker der med sedimentær klippe, efter at den gennemgår vejrforhold?
- At fange skyggen af en neptunsk måne
- Vipper tech-titaner på toppen af markedet?


