Et stof, der hjælper en reaktion, der finder sted, men det er ikke en aktiv del er en?
Her er hvorfor:
* katalysator: En katalysator er et stof, der fremskynder en kemisk reaktion uden at blive konsumeret i processen. Det giver en alternativ reaktionsvej med en lavere aktiveringsenergi, hvilket får reaktionen til at forekomme hurtigere.
* ikke en aktiv del: Katalysatorer bliver ikke en del af produkterne. De regenereres i slutningen af reaktionen, klar til at katalysere flere reaktioner.
Eksempler på katalysatorer:
* enzymer: Biologiske katalysatorer, der letter biokemiske reaktioner i levende organismer.
* metalkatalysatorer: Brugt i mange industrielle processer, såsom Haber-Bosch-processen til ammoniaksyntese.
* syrekatalysatorer: Bruges i forskellige reaktioner, herunder esterificering og dehydrering.
 Varme artikler
Varme artikler
-
 Kombinatorisk high-throughput-strategi foreslået til screening af hydrogenudviklingsreaktionskataly…Skematisk illustration af high-throughput boble screeningsmetode. Kredit:NIMTE En forskergruppe ledet af prof. Wang Junqiang ved Ningbo Institute of Materials Technology and Engineering (NIMTE) und
Kombinatorisk high-throughput-strategi foreslået til screening af hydrogenudviklingsreaktionskataly…Skematisk illustration af high-throughput boble screeningsmetode. Kredit:NIMTE En forskergruppe ledet af prof. Wang Junqiang ved Ningbo Institute of Materials Technology and Engineering (NIMTE) und -
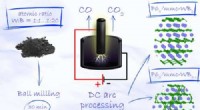 Superhård materialesyntese gjort billigereGrafisk abstrakt. Kredit:Uorganisk kemi (2022). DOI:10.1021/acs.inorgchem.1c03880 Skoltech-forskere og deres kolleger fra Tomsk Polytechnic University har foreslået en effektiv og billig måde at sy
Superhård materialesyntese gjort billigereGrafisk abstrakt. Kredit:Uorganisk kemi (2022). DOI:10.1021/acs.inorgchem.1c03880 Skoltech-forskere og deres kolleger fra Tomsk Polytechnic University har foreslået en effektiv og billig måde at sy -
 Miljøsikker rød blændingsraket skifter fyrværkeri, soldat teknologiAmerikanske og tyske forskere gik sammen om at udvikle et miljøvenligt rødt lys. Formlen er en lithiumbaseret pyroteknisk sammensætning af rødt lys af høj renhed og farvekvalitet, og undgår en liste o
Miljøsikker rød blændingsraket skifter fyrværkeri, soldat teknologiAmerikanske og tyske forskere gik sammen om at udvikle et miljøvenligt rødt lys. Formlen er en lithiumbaseret pyroteknisk sammensætning af rødt lys af høj renhed og farvekvalitet, og undgår en liste o -
 Video:Natto, den stinkende, slimet sojasnackKredit:The American Chemical Society Natto, en fødevare lavet af fermenterede sojabønner, slukker ofte nybegyndere til japansk mad på grund af dens stærke lugt og trævlede slim. Men mange mennesk
Video:Natto, den stinkende, slimet sojasnackKredit:The American Chemical Society Natto, en fødevare lavet af fermenterede sojabønner, slukker ofte nybegyndere til japansk mad på grund af dens stærke lugt og trævlede slim. Men mange mennesk
- Data fra elefantsæler afslører nye træk ved Blob-varmebølgen
- Undersøgelse viser positivt laboratoriemiljø, der er afgørende for bachelorsucces i forskning
- EU begynder blodig hård kamp for at nå grønne ambitioner
- Is oil called fossil fuel because it has fossils in it?
- Nøgle til styring af kunstvanding for bioenergiproduktion for at afbøde klimaændringer
- Ultrahurtige optiske feltioniserede gasser:En laboratorieplatform til undersøgelse af kinetiske pla…


