Når 2 væsker er blandet og varme udvikles, hvilken type opløsning dannes hvad er afvigelsen?
Afvigelsen fra ideel opførsel i dette tilfælde kaldes negativ afvigelse . Her er hvorfor:
* Ideelle løsninger: Ideelle løsninger antager, at ingen varme absorberes eller frigives under blanding (entalpi af opløsning er nul). De antager også ingen volumenændring ved blanding.
* negativ afvigelse: Når der frigøres varme (eksoterm), er de intermolekylære kræfter mellem opløsningsmiddel- og opløsningsmiddelmolekylerne stærkere end dem mellem de rene komponenter. Dette fører til en mere ordnet tilstand, et fald i volumen og en negativ entalpi af opløsning.
Eksempler på negative afvigelser:
* Blanding af svovlsyre (H₂so₄) og vand: Dette genererer betydelig varme, og får endda blandingen til at koge, hvis det ikke gøres omhyggeligt.
* Blanding af ethanol og vand: Dette frigiver også varme og fører til et fald i det samlede volumen.
Kortfattet:
* eksotermisk opløsning: Varmen frigøres.
* negativ afvigelse: Stærkere interaktioner mellem opløst stof og opløsningsmiddelmolekyler sammenlignet med de rene komponenter. Dette fører til en mere ordnet tilstand, et fald i volumen og en negativ entalpi af opløsning.
 Varme artikler
Varme artikler
-
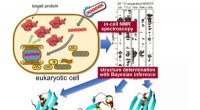 In-situ måling af 3-D proteinstruktur inde i levende eukaryote cellerMålproteiner udtrykkes indeni sf9 celler, derefter målt under anvendelse af in-cell NMR-spektroskopi. Unik statistisk analyse ved hjælp af Bayesiansk slutning anvendes til at beregne den nøjagtige
In-situ måling af 3-D proteinstruktur inde i levende eukaryote cellerMålproteiner udtrykkes indeni sf9 celler, derefter målt under anvendelse af in-cell NMR-spektroskopi. Unik statistisk analyse ved hjælp af Bayesiansk slutning anvendes til at beregne den nøjagtige -
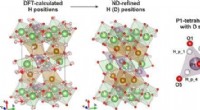 Forskere afslører kompleks defekt struktur af Li-ion katode materialeGrafisk abstrakt. Kredit: Uorganisk kemi (2021). DOI:10.1021/acs.inorgchem.0c03241 Skoltech-forskere har undersøgt hydroxyl-defekterne i LiFePO 4 , et meget udbredt katodemateriale i kommerciel
Forskere afslører kompleks defekt struktur af Li-ion katode materialeGrafisk abstrakt. Kredit: Uorganisk kemi (2021). DOI:10.1021/acs.inorgchem.0c03241 Skoltech-forskere har undersøgt hydroxyl-defekterne i LiFePO 4 , et meget udbredt katodemateriale i kommerciel -
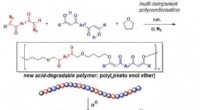 Ny syntetisk polymer nedbrydeligt under meget milde sure betingelserFremstilling af ny nedbrydelig syntetisk polymer. Kredit:Ehime University Et forskerhold ved Ehime University forberedte en ny type syntetisk polymer, som kan nedbrydes til en kombination af velde
Ny syntetisk polymer nedbrydeligt under meget milde sure betingelserFremstilling af ny nedbrydelig syntetisk polymer. Kredit:Ehime University Et forskerhold ved Ehime University forberedte en ny type syntetisk polymer, som kan nedbrydes til en kombination af velde -
 On-the-fly analyse af, hvordan katalysatorer ændrer sig under reaktioner for at forbedre ydeevnenEn skitse af den nye metode, der muliggør hurtig, on-the-fly bestemmelse af tredimensionel struktur af nanokatalysatorer. Det neurale netværk konverterer røntgenabsorptionsspektrene til geometrisk inf
On-the-fly analyse af, hvordan katalysatorer ændrer sig under reaktioner for at forbedre ydeevnenEn skitse af den nye metode, der muliggør hurtig, on-the-fly bestemmelse af tredimensionel struktur af nanokatalysatorer. Det neurale netværk konverterer røntgenabsorptionsspektrene til geometrisk inf
- Hvad sker der, når du lægger tøris i vand?
- Nøgleindikatorer opdaget for klimaændringernes indvirkning på vandforsyningen i Californien
- Hvad gør en ny tåge?
- Gennemgang af ædelgasspinforstærkning via spin-udvekslingskollisioner
- Hvordan definerer du had?
- Hvilken cellulær proces gør det muligt for forskellige dele af kroppen at udføre særlige funktio…


