Hvad er pH for rent vand ved 313 K, hvis kw den temperatur 2,917 x 10 -14?
forståelse af koncepterne
* kW (ionisk produkt af vand): KW er ligevægtskonstanten til auto-ionisering af vand:
`` `
2H₂O (L) ⇌ H₃O⁺ (aq) + OH⁻ (aq)
`` `
Kw =[h₃o⁺] [oh⁻]
* ph: pH er et mål for surhedsgraden eller alkaliniteten af en opløsning. Det er defineret som:
`` `
ph =-log [h₃o⁺]
`` `
Beregninger
1. Find [H₃O⁺]: Da rent vand er neutralt, [h₃o⁺] =[oh⁻]. Vi kan bruge KW til at løse til [H₃O⁺]:
`` `
Kw =[h₃o⁺] [oh⁻] =[h₃o⁺] ²
[H₃O⁺] =√kw =√ (2.917 x 10⁻¹⁴) =1,708 x 10⁻⁷ m
`` `
2. Beregn pH:
`` `
pH =-log [H₃O⁺] =-log (1,708 x 10⁻⁷) ≈ 6,77
`` `
Derfor er pH af rent vand ved 313 K ca. 6,77.
Vigtig note: Selvom pH er lidt mindre end 7, betragtes rent vand ved denne temperatur stadig som neutral. PH af rent vand er kun nøjagtigt 7 ved 298 K (25 ° C).
Sidste artikelStof, der ændrer hastigheden for kemiske reaktioner?
Næste artikelEr saltvand et rent stof?
 Varme artikler
Varme artikler
-
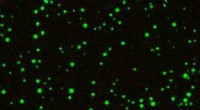 Forskere undersøger, hvordan forskellige flydende organeller i celler skabesSom stjerner i natten, flydende dråber af RNA (de lyse grønne kugler) flyder i en opløsning indeholdende høje koncentrationer af divalente magnesiumkationer. Dråberne afbildes gennem konfokal fluoresc
Forskere undersøger, hvordan forskellige flydende organeller i celler skabesSom stjerner i natten, flydende dråber af RNA (de lyse grønne kugler) flyder i en opløsning indeholdende høje koncentrationer af divalente magnesiumkationer. Dråberne afbildes gennem konfokal fluoresc -
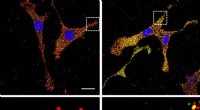 Billeddannelse af mRNA lige der, hvor det er lavet - på stedet for translationForskere bruger fluorescensprober til at overvåge stigninger i mRNA-ribosominteraktionsniveauer for et gen, der er forbundet med jernlagring som reaktion på jern (højre paneler). Målestok =20 μm. Kred
Billeddannelse af mRNA lige der, hvor det er lavet - på stedet for translationForskere bruger fluorescensprober til at overvåge stigninger i mRNA-ribosominteraktionsniveauer for et gen, der er forbundet med jernlagring som reaktion på jern (højre paneler). Målestok =20 μm. Kred -
 En ny strategi til at stabilisere carbonnitrid-fotokatalysator til nitrogenreduktion(a) TEM-billede af BCN; (b) UV-vis diffuse reflektansspektre, (c) steady-state PL-spektre, (d) forbigående fotostrømresponser og (e) N2-TPD af CN og BCN; (f) MD-simuleringssnapshots af BCN. Kredit:WAN
En ny strategi til at stabilisere carbonnitrid-fotokatalysator til nitrogenreduktion(a) TEM-billede af BCN; (b) UV-vis diffuse reflektansspektre, (c) steady-state PL-spektre, (d) forbigående fotostrømresponser og (e) N2-TPD af CN og BCN; (f) MD-simuleringssnapshots af BCN. Kredit:WAN -
 Computervision hjælper forskere med at studere lithium-ion-batterierEn ny computervisionsalgoritme til at identificere partikler i en lithium-ion batteri katode har hjulpet forskere med at spore katodens nedbrydning over tid. Kredit:Yijin Liu/SLAC National Accelerator
Computervision hjælper forskere med at studere lithium-ion-batterierEn ny computervisionsalgoritme til at identificere partikler i en lithium-ion batteri katode har hjulpet forskere med at spore katodens nedbrydning over tid. Kredit:Yijin Liu/SLAC National Accelerator
- Opstår der en fysisk eller kemisk ændring, når aluminiumsfolie anbringes i flydende brom og hvide…
- Nyt materiale kan forbedre sikkerheden for førstehjælpere over for kemiske farer
- Sådan virker antidepressiva
- Hvordan bruges termisk energi til maufakturering af industrielle anvendelser?
- Høj klimavariabilitet og stigende tørhed bragte en ende på en tidlig hominidart
- Hvordan skove mistede 8.000 års lagret kulstof på få generationer


