Hvordan adskiller smelte- og kogepunkterne i vand sig fra dem en sukker-vandopløsning?
smeltepunkt:
* rent vand: Smeltningspunktet for rent vand er 0 ° C (32 ° F) .
* sukker-vandopløsning: Smeltningspunktet for en sukker-vandopløsning er lavere end det for rent vand. Dette skyldes, at de opløste sukkermolekyler forstyrrer hydrogenbindingerne mellem vandmolekyler, hvilket gør det lidt lettere for løsningen at overgang fra et fast stof til en flydende tilstand. Den nøjagtige frysepunktdepression afhænger af koncentrationen af sukker.
Kogepunkt:
* rent vand: Kogepunktet for rent vand er 100 ° C (212 ° F) Ved standard atmosfærisk tryk.
* sukker-vandopløsning: Kogepunktet for en sukker-vandopløsning er højere end det for rent vand. Dette skyldes et fænomen kaldet kogepunkthøjde. De opløste sukkermolekyler skaber en højere koncentration af opløste partikler, hvilket kræver mere energi for at overvinde de intermolekylære kræfter og overgang til en gasformet tilstand. Jo højere koncentration af sukker er, jo højere er kogepunktforhøjelsen.
Nøglepunkter:
* Kolligative egenskaber: Depression af smeltepunkt og kogepunkthøjde er eksempler på kolligative egenskaber. Disse egenskaber afhænger udelukkende af antallet af opløste partikler opløst i et opløsningsmiddel, ikke af arten af disse partikler.
* Koncentration betyder noget: I hvilket omfang smeltepunktet er deprimeret, og kogepunktet er forhøjet afhænger af koncentrationen af sukkeropløsningen. Flere koncentrerede løsninger oplever en større ændring i disse egenskaber.
Fortæl mig, hvis du gerne vil have en mere detaljeret forklaring af et specifikt aspekt!
Sidste artikelEr opløsning af salt i vand en kemisk ændring?
Næste artikelHvilket molekyle kan nedbrydes i mindre molekyler?
 Varme artikler
Varme artikler
-
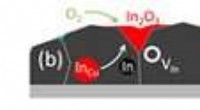 Spørgsmål og svar:Mod en ny måde at producere solceller påKredit:University of Luxembourg Fysikere fra University of Luxembourg sammen med internationale forskere har undersøgt oxidationsprocessen af solcellematerialer, hvis resultater kan ændre den nu
Spørgsmål og svar:Mod en ny måde at producere solceller påKredit:University of Luxembourg Fysikere fra University of Luxembourg sammen med internationale forskere har undersøgt oxidationsprocessen af solcellematerialer, hvis resultater kan ændre den nu -
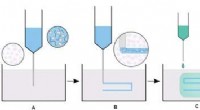 Ny 3-D printteknik til biomaterialerEt skema, der viser produktionen af et 3D bioprintet stillads ved brug af SLAM. A) Væskegel-printlejet skabes ved forskydningsafkøling af en varm agaroseopløsning gennem sol-gel-overgangen, som dere
Ny 3-D printteknik til biomaterialerEt skema, der viser produktionen af et 3D bioprintet stillads ved brug af SLAM. A) Væskegel-printlejet skabes ved forskydningsafkøling af en varm agaroseopløsning gennem sol-gel-overgangen, som dere -
 Ny katalysator gør styrenfremstilling billigere, grønnereKredit:North Carolina State University Kemiingeniørforskere har udviklet en ny katalysator, der markant øger udbyttet i styrenfremstilling, samtidig med at energiforbruget og drivhusgasemissionern
Ny katalysator gør styrenfremstilling billigere, grønnereKredit:North Carolina State University Kemiingeniørforskere har udviklet en ny katalysator, der markant øger udbyttet i styrenfremstilling, samtidig med at energiforbruget og drivhusgasemissionern -
 Udvideligt skum til 3D-udskrivning af store objekterKredit:CC0 Public Domain Det er en frustrerende begrænsning ved 3D-print:Udskrevne objekter skal være mindre end den maskine, der fremstiller dem. Kæmpe maskiner er upraktiske til at printe store
Udvideligt skum til 3D-udskrivning af store objekterKredit:CC0 Public Domain Det er en frustrerende begrænsning ved 3D-print:Udskrevne objekter skal være mindre end den maskine, der fremstiller dem. Kæmpe maskiner er upraktiske til at printe store
- Hvad er et ord, der betyder et område omgivet af vand?
- Enkelt nanoskala hybridsystem til undersøgelse af vakuumfluktuationsfeltet
- CO2-reduktion og økonomisk vækst:Kan de gå hånd i hånd?
- Hvorfor drejer planeterne i en cirkel og ikke flyder væk fra hinanden?
- Hvorfor står Kina over for rekordoversvømmelser?
- Forskere samarbejder om ny undersøgelse for at søge universet efter tegn på teknologiske civilisa…


