Er brintgas en ideel gas?
Ideelle gasforudsætninger:
* Punktpartikler: Ideelle gasser antages at være lavet af punktpartikler uden volumen. Hydrogenmolekyler er små, men de har en endelig størrelse.
* Ingen intermolekylære kræfter: Ideelle gasser antages at have ingen attraktive eller frastødende kræfter mellem molekyler. Hydrogenmolekyler har svage van der Waals -kræfter.
* perfekt elastiske kollisioner: Ideelle gasser antages at have kollisioner, der sparer energi. Ægte gaskollisioner kan involvere energioverførsel.
Hvorfor brint er tæt:
* lille størrelse: Hydrogenmolekyler er de mindste af alle diatomiske molekyler, hvilket giver deres volumenbidrag relativt lille.
* svage interaktioner: Hydrogenmolekyler har meget svage intermolekylære kræfter på grund af deres lave polariserbarhed.
* lav densitet: Ved lave tryk og høje temperaturer er molekylerne langt fra hinanden og minimerer interaktionseffekter.
Når brint afviger:
* Højt tryk: Ved høje tryk bliver molekylernes volumen signifikant i forhold til rummet mellem dem, hvilket forårsager afvigelser fra ideel opførsel.
* lave temperaturer: Ved lave temperaturer bliver de svage intermolekylære kræfter vigtigere, hvilket fører til afvigelser.
Konklusion:
Mens brintgas ikke er en ideel gas, nærmer den sig ideel opførsel under forhold med lavt tryk og høj temperatur . I mange praktiske situationer kan behandling af det som en ideel gas give en god tilnærmelse. For nøjagtige beregninger, især under ekstreme forhold, er det imidlertid vigtigt at overveje den ikke-ideelle opførsel af brint.
 Varme artikler
Varme artikler
-
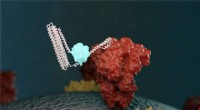 Nye biosensorer opdager hurtigt coronavirus -proteiner og antistofferEn illustration af en ny biosensor, der binder sig til et målrettet molekyle og udsender lys. Oprettelsen af biosensoren blev ledet af UW Medicine Institute for Protein Design. Kredit:Ian Haydon/UW
Nye biosensorer opdager hurtigt coronavirus -proteiner og antistofferEn illustration af en ny biosensor, der binder sig til et målrettet molekyle og udsender lys. Oprettelsen af biosensoren blev ledet af UW Medicine Institute for Protein Design. Kredit:Ian Haydon/UW -
 Hvorfor løg får os til at græde (og hvorfor nogle ikke gør det)Kredit:Shutterstock Mark Anthony i Shakespeares Cleopatra kan have henvist til tårerne, der lever i løget. Men hvorfor får løg os egentlig til at græde? Og hvorfor er det kun nogle løg, der får os
Hvorfor løg får os til at græde (og hvorfor nogle ikke gør det)Kredit:Shutterstock Mark Anthony i Shakespeares Cleopatra kan have henvist til tårerne, der lever i løget. Men hvorfor får løg os egentlig til at græde? Og hvorfor er det kun nogle løg, der får os -
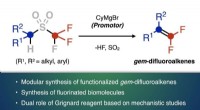 Etablering af en hurtig syntesemetode til nyttige organiske fluorforbindelserReaktionen af trifloner med det organiske magnesium-Grignard-reagens muliggør syntese af gem-difluoroalkenes Kredit:Issey Takahashi Nagoya University Institute of Transformative Bio-Molecules (W
Etablering af en hurtig syntesemetode til nyttige organiske fluorforbindelserReaktionen af trifloner med det organiske magnesium-Grignard-reagens muliggør syntese af gem-difluoroalkenes Kredit:Issey Takahashi Nagoya University Institute of Transformative Bio-Molecules (W -
 Tyndt lag beskytter batteriet, tillader kold opladningLagene i en lithiummetalanode til lavtemperaturbatterier Kredit:Donghai Wang, Penn State I jagten på en pålidelig, hurtig opladning, koldt vejr batteri til biler, en selvsamlende, et tyndt lag af
Tyndt lag beskytter batteriet, tillader kold opladningLagene i en lithiummetalanode til lavtemperaturbatterier Kredit:Donghai Wang, Penn State I jagten på en pålidelig, hurtig opladning, koldt vejr batteri til biler, en selvsamlende, et tyndt lag af
- Hvilken nukleinsyre forekommer som en dobbelt helix?
- Sådan konverteres europæiske højder til USAs
- Genbrugsforskning finder ny proces til at omdanne glasfiberforstærket plast til siliciumcarbid
- Neutrino-eksperiment hos Fermilab leverer en hidtil uset måling
- Bedre vandtest, mere sikre produkter
- hvad er peles egenskaber?


