Hvilken type binding dannes mellem fluor og silicium?
Her er hvorfor:
* Elektronegativitet: Fluor er det mest elektronegative element, mens silicium har en signifikant lavere elektronegativitet. Dette betyder, at fluor har en stærk attraktion for elektroner.
* Deling af elektroner: For at opnå en stabil elektronkonfiguration har fluor brug for endnu en elektron, og silicium har brug for fire. De deler elektroner i en kovalent binding, hvor begge atomer bidrager med elektroner til dannelse af et delt par.
* Polaritet: Mens bindingen er kovalent, resulterer den store forskel i elektronegativitet mellem fluor og silicium i en polær kovalent binding . De delte elektroner bruger mere tid tættere på fluoratomet, hvilket giver det en delvis negativ ladning og silicium en delvis positiv ladning.
Sidste artikelBalance ligning af Nano3 og KCL?
Næste artikelHvad er den naturlige tilstand af brom?
 Varme artikler
Varme artikler
-
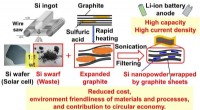 Fra skrald til skat:Siliciumaffald finder ny anvendelse i Li-ion-batterierFig. 1 Fremstilling af elektrode med Si-spåner/grafitpladekompositter (kredit:Osaka University) Li-ion-batterier (LIBer) er meget udbredt i mobilelektronik. Bekymringer for global opvarmning og kl
Fra skrald til skat:Siliciumaffald finder ny anvendelse i Li-ion-batterierFig. 1 Fremstilling af elektrode med Si-spåner/grafitpladekompositter (kredit:Osaka University) Li-ion-batterier (LIBer) er meget udbredt i mobilelektronik. Bekymringer for global opvarmning og kl -
 Kemikere designer minesystemer til at teste lægemiddelfunktionMillioner af små dråber i minesystemet kan genereres hurtigt til hurtigt antistoftest. Kredit:Lerner Lab / Scripps Research Forskere fra Scripps Research har løst et stort problem inden for kemi o
Kemikere designer minesystemer til at teste lægemiddelfunktionMillioner af små dråber i minesystemet kan genereres hurtigt til hurtigt antistoftest. Kredit:Lerner Lab / Scripps Research Forskere fra Scripps Research har løst et stort problem inden for kemi o -
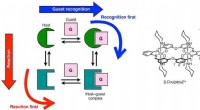 Styring af iongenkendelse i reaktive værts-gæstesystemerIllustration af scenarierne reaktion først og anerkendelse først i reaktive vært-gæst-systemer (til venstre) og værtsmolekylet og dets skematiske fremstilling, der bruges af Akine og kolleger (til høj
Styring af iongenkendelse i reaktive værts-gæstesystemerIllustration af scenarierne reaktion først og anerkendelse først i reaktive vært-gæst-systemer (til venstre) og værtsmolekylet og dets skematiske fremstilling, der bruges af Akine og kolleger (til høj -
 Forskere laver kraftfuld undervandslim inspireret af havbarn og muslingerModelfly monteret med silkebaseret lim. Kredit:Marco Lo Presti, Tufts University Hvis du nogensinde har prøvet at hugge en musling ud af en havmur eller et fjeder af bunden af en båd, du vil for
Forskere laver kraftfuld undervandslim inspireret af havbarn og muslingerModelfly monteret med silkebaseret lim. Kredit:Marco Lo Presti, Tufts University Hvis du nogensinde har prøvet at hugge en musling ud af en havmur eller et fjeder af bunden af en båd, du vil for
- Hvor er ledende metaller nyttige i livet?
- Lunar Gateway vil bevare sin bane med en 6 kW ionmotor
- Forskere finder mønstre forbundet med ekstreme oversvømmelser
- Blive eller gå? Vulkan tvinger valgmuligheder for alle i udbrudszonen
- Hvad er 236lb i kilogram?
- Fra handel med stoffer til salg af tortillas:Den overraskende fremtid for tidligere bandemedlemmer


