Hvad menes med natriumacetat et grundlæggende salt?
1. Hydrolyse af anionen:
- Natriumacetat i opløsning dissocieres i natriumioner (Na+) og acetationer (ch₃coo-).
- Acetationen, der er den konjugatbase af en svag syre (eddikesyre, ch₃cooh), gennemgår hydrolyse i vand.
- Det reagerer med vandmolekyler for at producere hydroxidioner (OH-) og eddikesyre:
`` `
Ch₃coo⁻ + h₂o ⇌ ch₃cooh + oh⁻
`` `
- Produktionen af hydroxidioner gør løsningen grundlæggende.
2. Opløsningens pH:
- Hydrolyse af acetationer fører til en stigning i hydroxidionkoncentrationen, hvilket resulterer i en pH -værdi på større end 7.
- En pH større end 7 indikerer en grundlæggende løsning.
3. Salt af stærk base og svag syre:
- Natriumacetat dannes ud fra reaktionen af en stærk base (natriumhydroxid, NaOH) og en svag syre (eddikesyre, ch₃cooh).
- Salte dannet fra en stærk base og en svag syre er typisk basale.
Kortfattet:
Natriumacetat betragtes som et grundlæggende salt på grund af hydrolyse af dets acetatanion, der producerer hydroxidioner og øger pH -værdien. Dannelsen af en grundlæggende opløsning er et kendetegn ved salte dannet fra en stærk base og en svag syre.
 Varme artikler
Varme artikler
-
 Video:Hvordan kemi gør fjernelse af kuldioxid muligKredit:The American Chemical Society I løbet af de sidste par hundrede år, mængden af kuldioxid i vores atmosfære er steget i vejret. Hvis vi ikke fjerner i det mindste noget af det, der kommer
Video:Hvordan kemi gør fjernelse af kuldioxid muligKredit:The American Chemical Society I løbet af de sidste par hundrede år, mængden af kuldioxid i vores atmosfære er steget i vejret. Hvis vi ikke fjerner i det mindste noget af det, der kommer -
 Hvedegluten viste sig at genoprette bindinger i skørt menneskehårKredit:Laura Tiitto/public domain Et team af forskere fra Jiangnan University i Kina og University of Nebraska i USA har fundet ud af, at integrering af hvedegluten i en shampoo hjælper med at gen
Hvedegluten viste sig at genoprette bindinger i skørt menneskehårKredit:Laura Tiitto/public domain Et team af forskere fra Jiangnan University i Kina og University of Nebraska i USA har fundet ud af, at integrering af hvedegluten i en shampoo hjælper med at gen -
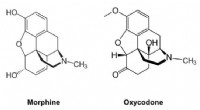 Design af mindre vanedannende opioider gennem kemiMorfin, oxycodon, og hydrocodon tilhører samme klasse af opioider og har lignende strukturer. Kredit:Aaron Harrison, CC BY-ND Hvad hvis der var en måde for smertepatienter at få al den smertelindr
Design af mindre vanedannende opioider gennem kemiMorfin, oxycodon, og hydrocodon tilhører samme klasse af opioider og har lignende strukturer. Kredit:Aaron Harrison, CC BY-ND Hvad hvis der var en måde for smertepatienter at få al den smertelindr -
 Kigger ind i flammerne fra ioniske vindeKredit:King Abdullah University of Science and Technology Nye 3D-visualiseringer, der afslører, hvordan flammer reagerer på elektriske felter, kan hjælpe med at forbedre forbrændingseffektiviteten
Kigger ind i flammerne fra ioniske vindeKredit:King Abdullah University of Science and Technology Nye 3D-visualiseringer, der afslører, hvordan flammer reagerer på elektriske felter, kan hjælpe med at forbedre forbrændingseffektiviteten
- Hvad synes forskere om kernen i Uranus?
- Hvilke to faktorer påvirker den temperatur, der klipper, smelter ved?
- Hvordan sætter man et skarpt atomur model spc 502 op?
- Hvad er månens lysstyrke, der driver en aftagende gibbous?
- Tal begrænser, hvor præcist digitale computere modellerer kaos
- Hvordan slippe af med Groundhogs, Moles og Gophers


