Hvilken forbindelse produceres, når 6,08 g nitrogen kombineres med 13,92 ilt?
1. Bestem molen for hvert element:
* nitrogen (n):
* Molmasse på n =14,01 g/mol
* Mol n =6,08 g / 14,01 g / mol =0,434 mol
* ilt (O):
* Molmasse på O =16,00 g/mol
* Mol O =13,92 g / 16,00 g / mol =0,870 mol
2. Find molforholdet:
* Opdel molen for hvert element med det mindste antal mol (0,434 mol i dette tilfælde):
* N:0,434 mol / 0,434 mol =1
* O:0,870 mol / 0,434 mol ≈ 2
3. Bestem den empiriske formel:
* Molforholdet indikerer, at forbindelsen har 1 nitrogenatom for hvert 2 iltatomer.
* Den empiriske formel er n₂o₄ , som er dinitrogen tetroxid .
Vigtig note: Dinitrogen -tetroxid er en meget reaktiv forbindelse. I den virkelige verden vil det sandsynligvis være i ligevægt med nitrogendioxid (NO₂).
 Varme artikler
Varme artikler
-
 Forskere introducerer idé til nye molekyler, innovation, værdiLedere fra National Science Foundation Engineering Research Center for Biorenewable Chemicals (CBiRC) baseret på Iowa State University foreslår en ny model til at skabe, ansøger, og kommercialisering
Forskere introducerer idé til nye molekyler, innovation, værdiLedere fra National Science Foundation Engineering Research Center for Biorenewable Chemicals (CBiRC) baseret på Iowa State University foreslår en ny model til at skabe, ansøger, og kommercialisering -
 Scanner til malerier viser sig at være et lovende nyt CSI -værktøjFire forskellige blodpletter på en sort T-shirt, synliggjort ved hjælp af MA-XRF på basis af jern- og kaliumsignalet. Kredit:Delft University of Technology Et forskningssamarbejde har introduceret
Scanner til malerier viser sig at være et lovende nyt CSI -værktøjFire forskellige blodpletter på en sort T-shirt, synliggjort ved hjælp af MA-XRF på basis af jern- og kaliumsignalet. Kredit:Delft University of Technology Et forskningssamarbejde har introduceret -
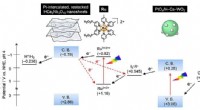 Ny fotokatalysator øger vandspaltningseffektiviteten til ren brintproduktionOxygenudviklingskatalysatoren reducerer effektivt koncentrationen af I3 - ioner og ændringer i hydrogenudviklingskatalysatoren forhindrer elektrontilbageførsel (stiplede røde linjer) og prioriterer
Ny fotokatalysator øger vandspaltningseffektiviteten til ren brintproduktionOxygenudviklingskatalysatoren reducerer effektivt koncentrationen af I3 - ioner og ændringer i hydrogenudviklingskatalysatoren forhindrer elektrontilbageførsel (stiplede røde linjer) og prioriterer -
 Nyt tilsætningsstof hjælper forskere mere selektivt med at omdanne CO2 til brændstoffer med flere…Illustration af kunstig fotosyntese, en proces, hvor sollys, CO2, og vand omdannes i laboratorier til nyttige brændstoffer. Dette er hovedmålet for Joint Center for Artificial Photosynthesis (JCAP), e
Nyt tilsætningsstof hjælper forskere mere selektivt med at omdanne CO2 til brændstoffer med flere…Illustration af kunstig fotosyntese, en proces, hvor sollys, CO2, og vand omdannes i laboratorier til nyttige brændstoffer. Dette er hovedmålet for Joint Center for Artificial Photosynthesis (JCAP), e
- Er en beskrivelse af Orbits -stierne de fleste planeter i dit solsystem?
- Græsarealer rummer potentiale for øget fødevareproduktion
- Hvad er skjult i en klippe, der indeholder olie?
- Bohr-modellen:Hurtigt udskiftet, men aldrig glemt
- Hvad er den metamorfe kvalitet af gneis?
- At stole på GPS forhindrer dele af din hjerne i at blive aktiveret


