Hvor mange kilogram kobbersulfid kunne dannes fra reaktion 0,90 mol med overskydende svovl?
1. Afbalanceret kemisk ligning:
Reaktionen af kobber (Cu) med svovl (er) til dannelse af kobbersulfid (CUS) er:
Cu + s → cus
Denne ligning er allerede afbalanceret.
2. Molforhold:
Fra den afbalancerede ligning ser vi, at 1 mol Cu reagerer med 1 mol S for at producere 1 mol CUS.
3. Beregn mol af kobbersulfid:
Da du har 0,90 mol Cu, og det reagerer i et forhold på 1:1 mol med CUS, producerer du 0,90 mol CUS.
4. Konverter mol til kilogrammer:
* Find den molære masse af CUS:
* CU:63,55 g/mol
* S:32,06 g/mol
* CUS:63,55 + 32,06 =95,61 g/mol
* Konverter mol Cus til gram:
* 0,90 mol cus * 95,61 g/mol =86,05 g cus
* Konverter gram til kilogram:
* 86,05 g Cus * (1 kg / 1000 g) =0,08605 kg CUS
Svar: Du kan danne 0,08605 kg af kobbersulfid fra reaktionen af 0,90 mol kobber med overskydende svovl.
 Varme artikler
Varme artikler
-
 Mobil, øjeblikkelig diagnose af viraEn ny teknik vil gøre det muligt at opdage vira i marken. I dette tilfælde, et yam-grund i Guadeloupe. Kredit:D. Filloux, Cirad I en første for plantevirologi, et hold fra CIRAD brugte for nylig n
Mobil, øjeblikkelig diagnose af viraEn ny teknik vil gøre det muligt at opdage vira i marken. I dette tilfælde, et yam-grund i Guadeloupe. Kredit:D. Filloux, Cirad I en første for plantevirologi, et hold fra CIRAD brugte for nylig n -
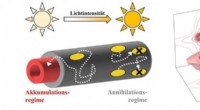 Energiflow i nanoområdetKredit:Billeder:Björn Kriete (v.) / Stefan Mueller (r.) Planter og bakterier kan fange sollysets energi med lys-høstende antenner og overføre den til et reaktionscenter. At transportere energi eff
Energiflow i nanoområdetKredit:Billeder:Björn Kriete (v.) / Stefan Mueller (r.) Planter og bakterier kan fange sollysets energi med lys-høstende antenner og overføre den til et reaktionscenter. At transportere energi eff -
 Ny indsigt afsløret gennem århundredgammel fotokemiteknikTætbundne ionpar reorganiseres efter fotoexcitation for at minimere det samlede dipolmoment, hvilket kan blokere specifikke typer elektronoverførselsreaktioner. Kredit:Justin Earley, NREL Som digte
Ny indsigt afsløret gennem århundredgammel fotokemiteknikTætbundne ionpar reorganiseres efter fotoexcitation for at minimere det samlede dipolmoment, hvilket kan blokere specifikke typer elektronoverførselsreaktioner. Kredit:Justin Earley, NREL Som digte -
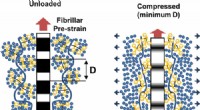 Kollagen i bruskvæv opfører sig som flydende krystaller på en smartphone-skærmKredit:ACS Brusk i vores led indeholder kollagen, som opfører sig lidt som de flydende krystaller på en smartphones skærm, ifølge forskere ved Queen Mary University of London (QMUL). Kollagenet æ
Kollagen i bruskvæv opfører sig som flydende krystaller på en smartphone-skærmKredit:ACS Brusk i vores led indeholder kollagen, som opfører sig lidt som de flydende krystaller på en smartphones skærm, ifølge forskere ved Queen Mary University of London (QMUL). Kollagenet æ
- NASAs Saturn-kredsende Cassini-rumfartøj står over for en brændende finish
- CERN -eksperiment forbedrer præcisionen af antiproton -massemåling med ny innovativ køleteknik
- Hvorfor er ilt vigtigt for vand?
- Ingeniører udvikler kræftmålrettede nanoprobe-sensorer
- Adfærdsmæssige tilpasninger af Giraffes
- Hvordan man adresserer Amerika fører til krise og giver sikkert drikkevand til alle


