Separationsteknik af natriumchlorid fra dets opløsning i vand?
1. Opvarmning: Løsningen opvarmes forsigtigt. Dette giver energi til vandmolekylerne, hvilket får dem til at få kinetisk energi og bevæge sig hurtigere.
2. fordampning: Efterhånden som vandmolekylerne får nok energi, overvinder de de attraktive kræfter, der holder dem i flydende tilstand og undslipper i luften som vanddamp.
3. Krystallisation: Når vand fordamper, øges koncentrationen af natriumchlorid i den resterende opløsning. Til sidst bliver opløsningen mættet, hvilket betyder, at den ikke kan holde mere opløst salt. På dette tidspunkt begynder natriumchloridet at krystallisere ud af opløsningen som faste krystaller.
4. samling: De faste natriumchloridkrystaller kan opsamles og tørres for at fjerne eventuelle resterende spor af vand.
Andre metoder:
* destillation: Dette involverer kogning af opløsningen og opsamling af vanddampen separat, hvilket efterlader natriumchloridet. Dette er mere energikrævende end fordampning.
* solfordampning: Dette er en mindre præcis metode ved hjælp af solens varme til at fordampe vandet. Det er velegnet til storstilet saltproduktion fra havvand.
Vigtig note: Valget af metode afhænger af skalaen for adskillelsen, saltens ønskede renhed og de tilgængelige ressourcer.
Sidste artikelOrdligning til reaktion af halogener med natrium?
Næste artikelHvorfor kan et iltatom ikke danne en tredobbelt binding?
 Varme artikler
Varme artikler
-
 Generering af strøm fra forurenet luftDen nye enhed må kun udsættes for lys for at rense luft og generere strøm. Kredit:UAntwerpen og KU Leuven Forskere fra University of Antwerpen og KU Leuven (University of Leuven), Belgien, har udv
Generering af strøm fra forurenet luftDen nye enhed må kun udsættes for lys for at rense luft og generere strøm. Kredit:UAntwerpen og KU Leuven Forskere fra University of Antwerpen og KU Leuven (University of Leuven), Belgien, har udv -
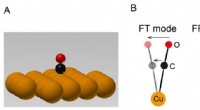 Belysning af vibrationsenergi af et enkelt molekyle i et eksternt kraftfeltFigur 1A:Skematisk billede af et enkelt CO-molekyle i ensomhed adsorberet på en enkelt kobberkrystal. 1B:Skematiske billeder af vibrationer af et CO-molekyle adsorberet på en kobberoverflade. Et CO-mo
Belysning af vibrationsenergi af et enkelt molekyle i et eksternt kraftfeltFigur 1A:Skematisk billede af et enkelt CO-molekyle i ensomhed adsorberet på en enkelt kobberkrystal. 1B:Skematiske billeder af vibrationer af et CO-molekyle adsorberet på en kobberoverflade. Et CO-mo -
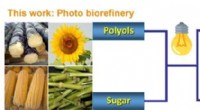 Ny fotokatalytisk metode omdanner biopolyoler og sukkerarter til methanol og syngasMetanol og syngas fungerer som platformskemikaliet, der forbinder bioraffinaderiet og petrokemisk industri. Kredit:WANG Min En forskergruppe ledet af prof. Wang Feng fra Dalian Institute of Chemic
Ny fotokatalytisk metode omdanner biopolyoler og sukkerarter til methanol og syngasMetanol og syngas fungerer som platformskemikaliet, der forbinder bioraffinaderiet og petrokemisk industri. Kredit:WANG Min En forskergruppe ledet af prof. Wang Feng fra Dalian Institute of Chemic -
 Forskere udvikler nyt system til undersøgelse af nye krydsbårne sygdommeKredit:stock.adobe.com Krydsbårne sygdomme er stigende, og især en dukker op i USA og Canada. Human babesiose er en infektion, der kan forårsage en række symptomer og endda døden. Lidt er kendt om
Forskere udvikler nyt system til undersøgelse af nye krydsbårne sygdommeKredit:stock.adobe.com Krydsbårne sygdomme er stigende, og især en dukker op i USA og Canada. Human babesiose er en infektion, der kan forårsage en række symptomer og endda døden. Lidt er kendt om
- Hvad med den største indflydelse på alle genstande inden for Mælkevej kaldes hvad?
- Hvordan Einsteins gravitationsteori oplevede en renæssance efter Anden Verdenskrig
- Er en godt kogt bøf kemikalie eller fysisk forandring?
- The Glass Armonica:A Harmonious Invention af Benjamin Franklin
- Globale klimamodeller for folkesundhed? Nyttig, men ikke på den måde, vi tror
- Hvilken slags ting kan ordnes ved hjælp af erstatningsglas?


