Hvis et stof gennemgår faseændring, hvad sker der?
Hvad sker der under en faseændring:
* Energioverførsel: Faseændringer involverer altid enten absorption eller frigivelse af energi.
* Absorption: Når et stof absorberer energi (som varme), bevæger dets molekyler sig hurtigere og slipper fri fra deres bindinger, hvilket forårsager en faseændring til en mindre tæt tilstand (fast til væske, væske til gas).
* Udgivelse: Når et stof frigiver energi, bremser dets molekyler og binder sig stærkere, hvilket fører til en faseændring til en tættere tilstand (gas til væske, væske til fast).
* Ændringer i fysiske egenskaber:
* densitet: Faststoffer er tættere end væsker, og væsker er tættere end gasser.
* form: Faststoffer har en fast form, væsker har formen på deres beholder, og gasser fylder deres beholder helt.
* bind: Mængden af et stof kan ændres under en faseændring. For eksempel udvides vand, når det fryser.
Typer af faseændringer:
* smeltning: Solid til væske (absorption af energi)
* Frysning: Væske til fast stof (frigivelse af energi)
* fordampning: Væske til gas (absorption af energi)
* kondens: Gas til væske (frigivelse af energi)
* sublimering: Fast til gas (absorption af energi)
* afsætning: Gas til fast (frigivelse af energi)
Eksempel:
Forestil dig en blok af is (fast vand) ved 0 ° C. Hvis du tilsætter varme, smelter isen og bliver flydende vand. Dette skyldes, at varmeenergien får vandmolekylerne til at bevæge sig hurtigere og bryde fri fra deres stive struktur. Hvis du fortsætter med at tilsætte varme, koger det flydende vand til sidst og bliver vanddamp (gas).
Nøglepunkter:
* Faseændringer er fysiske ændringer , ikke kemiske ændringer. Stofets kemiske sammensætning forbliver den samme.
* Faseændringer er reversible . Du kan ændre et stof tilbage til sin oprindelige tilstand ved at tilføje eller fjerne energi.
* Faseændringer er vigtige i mange naturlige processer, såsom vandcyklus og vejrmønstre.
 Varme artikler
Varme artikler
-
 Forskere gør et vigtigt fremskridt i retning af produktion af vigtigt biobrændstofGrafisk, der viser biobutanolseparationsmetode. Kredit:Oregon State University Et internationalt forskningssamarbejde har taget et vigtigt skridt i retning af den kommercielt levedygtige fremstill
Forskere gør et vigtigt fremskridt i retning af produktion af vigtigt biobrændstofGrafisk, der viser biobutanolseparationsmetode. Kredit:Oregon State University Et internationalt forskningssamarbejde har taget et vigtigt skridt i retning af den kommercielt levedygtige fremstill -
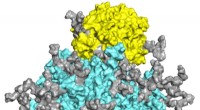 Ofte overset, molekyler kaldet glykaner regulerer COVID-19-spidsproteinfunktionenEn molekylær model viser det stærkt glykosylerede SARS-CoV-2-spidsprotein (cyan, med glykaner i grå og andre farver) bundet til den cellulære ACE2-receptor (gul). En ny undersøgelse fremhæver den krit
Ofte overset, molekyler kaldet glykaner regulerer COVID-19-spidsproteinfunktionenEn molekylær model viser det stærkt glykosylerede SARS-CoV-2-spidsprotein (cyan, med glykaner i grå og andre farver) bundet til den cellulære ACE2-receptor (gul). En ny undersøgelse fremhæver den krit -
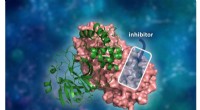 Historien om indsigtsfuld HIV-forskning inspirerer neutronspredningstilgang til at studere COVID-19Den tredimensionelle struktur af SARS-CoV-2 hovedproteasen. Det molekylære dimerkompleks består af en enkelt monomer (grøn) bundet til en anden monomer (lyserød), hvor en lægemiddelinhibitor vil binde
Historien om indsigtsfuld HIV-forskning inspirerer neutronspredningstilgang til at studere COVID-19Den tredimensionelle struktur af SARS-CoV-2 hovedproteasen. Det molekylære dimerkompleks består af en enkelt monomer (grøn) bundet til en anden monomer (lyserød), hvor en lægemiddelinhibitor vil binde -
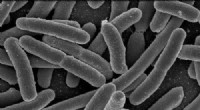 Knækning af colibactins kode:Undersøgelse undersøger, hvordan sammensatte beskadigede DNA for at …Escherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH I mere end et årti, forskere har arbejdet på at forstå sammenhængen mellem colibactin, en forbindelse fremstillet af visse stammer
Knækning af colibactins kode:Undersøgelse undersøger, hvordan sammensatte beskadigede DNA for at …Escherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH I mere end et årti, forskere har arbejdet på at forstå sammenhængen mellem colibactin, en forbindelse fremstillet af visse stammer
- Findes granit og basalt i vulkaner?
- Astronaut Michael Collins, Apollo 11 pilot, død af kræft
- Hvad er to eksempler på, hvordan anaerob respiration bruges i fødevare- og drikkevareindustrien?
- Bredbladede træer viser reduceret følsomhed over for global opvarmning
- Undersøgelse finder nye funktioner i babysnak på ethvert sprog
- Innovativ silicium nanochip kan omprogrammere biologisk væv i levende krop


