Hvad er den procentvise sammensætning af hvert element, der findes i ammoniumsulfid?
1. Bestem den molekylære formel:
* Ammoniumsulfid har formlen (NH₄) ₂s.
2. Beregn den molære masse:
* Nitrogen (n):2 atomer * 14,01 g/mol =28,02 g/mol
* Hydrogen (H):8 atomer * 1,01 g/mol =8,08 g/mol
* Svovl (er):1 atom * 32,07 g/mol =32,07 g/mol
* Total molmasse =68,17 g/mol
3. Beregn den procentvise sammensætning af hvert element:
* nitrogen (n): (28,02 g/mol/68,17 g/mol) * 100% = 41,11%
* brint (H): (8,08 g/mol/68,17 g/mol) * 100% = 11,86%
* svovl (er): (32,07 g/mol/68,17 g/mol) * 100% = 47,03%
Derfor er den procentvise sammensætning af ammoniumsulfid:
* nitrogen:41,11%
* brint:11,86%
* svovl:47,03%
Sidste artikelHvilket lag af atmosfæren har den højeste tæthedsgasmolekyler?
Næste artikelEr ammoniumhydroxid en ikke flygtig væske?
 Varme artikler
Varme artikler
-
 Opdagelse kan føre til et nyt katalysatordesign for at reducere nitrogenoxider i dieseludstødningDette diagram viser en ny reaktionsmekanisme, der kan bruges til at forbedre katalysatordesign til forureningsbekæmpelsessystemer til dieseludstødning. Kredit:Purdue University /Maureen Lifton For
Opdagelse kan føre til et nyt katalysatordesign for at reducere nitrogenoxider i dieseludstødningDette diagram viser en ny reaktionsmekanisme, der kan bruges til at forbedre katalysatordesign til forureningsbekæmpelsessystemer til dieseludstødning. Kredit:Purdue University /Maureen Lifton For -
 Innovationspionerer scorer verdens først for bæredygtigt byggeri med grafenbetonTeam fra University of Manchester og Nationwide Engineering om verdens første konstruerede grafenbeton i kommercielle omgivelser, kun et par kilometer øst for det gamle monument i Stonehenge, det nye
Innovationspionerer scorer verdens først for bæredygtigt byggeri med grafenbetonTeam fra University of Manchester og Nationwide Engineering om verdens første konstruerede grafenbeton i kommercielle omgivelser, kun et par kilometer øst for det gamle monument i Stonehenge, det nye -
 At få fermenterede mejeriprodukter til at smage bedreEmmental ost. Kredit:Wikipedia Forskere ved det tekniske universitet i München (TUM), Leibniz-instituttet for fødevaresystembiologi, og University of Hohenheim har udviklet en ny metodisk tilgang
At få fermenterede mejeriprodukter til at smage bedreEmmental ost. Kredit:Wikipedia Forskere ved det tekniske universitet i München (TUM), Leibniz-instituttet for fødevaresystembiologi, og University of Hohenheim har udviklet en ny metodisk tilgang -
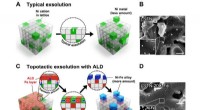 Ny katalysator forvandler drivhusgasser til brintgasFigur 1. Skematisk sammenligning, SEM billeder, korrelationen mellem antallet af ALD-cyklusser og partikelstørrelsen/populationen, og røntgenfotoelektronkurver for prøverne. (A) Konventionel løsning f
Ny katalysator forvandler drivhusgasser til brintgasFigur 1. Skematisk sammenligning, SEM billeder, korrelationen mellem antallet af ALD-cyklusser og partikelstørrelsen/populationen, og røntgenfotoelektronkurver for prøverne. (A) Konventionel løsning f
- Farlige vindkulde, sne i Midtvesten; kolde greb Nordøst
- Demonstrerer 2-D monolags transistorer med høj ydeevne på papirsubstrater
- Hvilken fosfatbinding er brudt i ATP for at forårsage frigivelse af fri energi?
- I DFW Lufthavn, dit ansigt kan en dag erstatte dit boardingkort
- Aramco ser lokal børsnotering, kan stige oversøisk notering:rapport
- Sådan konverteres Square Tommer til Cubic Feet


