Hvad er de tre mekanismer til fjernelse af hydrogenion?
1. buffering: Dette er den øjeblikkelige respons på ændringer i pH. Buffere er kemiske systemer, der modstår ændringer i pH ved at acceptere eller donere H+ -ioner. Eksempler inkluderer:
* bicarbonatbuffer System: Dette er det vigtigste buffersystem i blodet, hvor bicarbonationer (HCO3-) kan acceptere H+ til dannelse af kulsyre (H2CO3).
* phosphatbuffer System: Dette system er vigtigt i intracellulære væsker og involverer phosphationer (HPO42- og H2PO4-).
* Proteinbuffer System: Proteiner i blodet og cellerne kan fungere som buffere på grund af deres aminosyresammensætning.
2. respiratorisk regulering: Lungerne spiller en vigtig rolle i H+ fjernelse ved at regulere kuldioxid (CO2) niveauer i blodet.
* CO2 opløses i blod og reagerer med vand til dannelse af kulsyre (H2CO3), som derefter adskiller sig i H+ og bicarbonationer (HCO3-).
* Ved at øge ventilation (åndedrætsfrekvens og dybde) udviser lungerne mere CO2, reducerer H+ -koncentrationen og hæver pH. Omvendt bevarer faldende ventilation CO2, øger H+ og sænker pH.
3. Nyreforordning: Nyrerne er de primære organer, der er ansvarlige for langvarige pH-regulering. De opnår dette af:
* reabsorbering af bicarbonationer (HCO3-) :Nyrerne reabserer aktivt HCO3- fra filtratet, hvilket effektivt fjerner H+ fra blodet.
* udskiller H+ ioner :Nyrerne udskiller H+ i urinen, hvilket i sidste ende eliminerer den fra kroppen.
* Udskillelse af syrer: Nyrerne kan udskille faste syrer (f.eks. Mælkesyre, svovlsyre), der ikke er flygtige som CO2 og ikke kan fjernes af lungerne.
Disse tre mekanismer fungerer sammen for at opretholde en stabil pH inden for en meget smal rækkevidde, afgørende for korrekt funktion af kroppens celler, enzymer og organsystemer.
 Varme artikler
Varme artikler
-
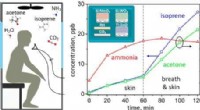 Bærbar enhed til at snuse ud fangede menneskerKredit:American Chemical Society Det første trin efter bygninger kollapsede fra et jordskælv, bombning eller anden katastrofe er at redde mennesker, der kunne blive fanget i murbrokkerne. Men at f
Bærbar enhed til at snuse ud fangede menneskerKredit:American Chemical Society Det første trin efter bygninger kollapsede fra et jordskælv, bombning eller anden katastrofe er at redde mennesker, der kunne blive fanget i murbrokkerne. Men at f -
 Forskere bestemmer aktive steder af Cu-znO-katalysatorer til vandgasskift og CO-hydrogeneringsreakti…Fig. 1:Mikroskopiske karakteriseringer. Skalabjælkerne for (a1–a3), (d1-d3), og (e1–e3) svarer til 500 nm, det for b3 svarer til 100 nm, dem af b1, b2, c2, og c3 svarer til 50 nm, det for c1 svarer ti
Forskere bestemmer aktive steder af Cu-znO-katalysatorer til vandgasskift og CO-hydrogeneringsreakti…Fig. 1:Mikroskopiske karakteriseringer. Skalabjælkerne for (a1–a3), (d1-d3), og (e1–e3) svarer til 500 nm, det for b3 svarer til 100 nm, dem af b1, b2, c2, og c3 svarer til 50 nm, det for c1 svarer ti -
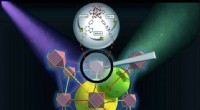 Brug porøse krystaller til at høste lysDen metalorganiske ramme (MOF) indeholder zirconiumbaserede knuder (lilla cuboctahedra) forbundet med kulstofbaserede linkermolekyler (røde og gule stænger) for at danne en porøs struktur med to store
Brug porøse krystaller til at høste lysDen metalorganiske ramme (MOF) indeholder zirconiumbaserede knuder (lilla cuboctahedra) forbundet med kulstofbaserede linkermolekyler (røde og gule stænger) for at danne en porøs struktur med to store -
 C9h -peptid er begrænset til at fremkalde kræftcelle -apoptoseKredit:Asociación RUVID Forskere ved Valencias Universitat Politècnica (UPV), Valencia-CSIC Biomedicine Institute (IBV) og Bioengineering, Biomateriale og nanomedicin CIBER (CIBER BBN) har udvikle
C9h -peptid er begrænset til at fremkalde kræftcelle -apoptoseKredit:Asociación RUVID Forskere ved Valencias Universitat Politècnica (UPV), Valencia-CSIC Biomedicine Institute (IBV) og Bioengineering, Biomateriale og nanomedicin CIBER (CIBER BBN) har udvikle
- Hvad er hydrogenerede olier lavet af?
- Tilsluttede biler kan lyve, udgør en ny trussel mod smarte byer
- Er 32 liter større end 9 gallon?
- Heliummangel! Hvad hvis vi løb tør for helium?
- Fracking og jordskælv - afvejer farerne i Sydafrika
- Forskere udvikler den første model til vejledning i storstilet produktion af ultratyndt grafen


