Elektronprikdiagram til svovl 8 molekyle?
forståelse af strukturen
* Svovls valenselektroner: Svovl har 6 valenselektroner.
* octet regel: Svovlatomer har en tendens til at dele elektroner for at opnå en stabil octet (8 valenselektroner).
* S8 Struktur: I S8-molekylet danner svovlatomerne en kroneformet ring, hvor hvert svovlatom er bundet til to andre svovlatomer.
Elektron dot diagramrepræsentation
Desværre repræsenterer et traditionelt elektronprikdiagram ikke fuldt ud 3D -strukturen af S8. Her er en forenklet repræsentation, der fokuserer på bindingen:
1. Start med svovlatomet: Repræsenterer hvert svovlatom med dets symbol (er) omgivet af seks prikker, der repræsenterer dets valenselektroner:
`` `
...
:S:
...
`` `
2. dannelse af obligationer: Hvert svovlatom danner to enkeltbindinger med to andre svovlatomer. Disse bindinger er repræsenteret ved at dele par prikker mellem svovlatomer.
`` `
.. ..
:S:..:S:
.. ..
`` `
3. Tilslutning af ringen: Dette mønster fortsætter omkring ringen og danner en lukket kæde:
`` `
.. ..
..:S:..:S:..
.. .. ..
:S:..:S:..:S:
.. .. ..
.. ..
`` `
vigtige noter
* Dette er en forenklet repræsentation, ikke en præcis 3D -model.
* Den virkelige struktur af S8 har svovlatomer arrangeret i en pucket, kroneformet ring.
* Elektronprikdiagrammer bruges primært til enkle molekyler. Mere komplekse molekyler som S8 er ofte repræsenteret med mere detaljerede strukturelle formler.
Fortæl mig, hvis du har yderligere spørgsmål!
Sidste artikelEr natrium et rent stof eller en blanding?
Næste artikelHvorfor er kobbernitrat og svovl den samme farve?
 Varme artikler
Varme artikler
-
 Ny forskning kan hjælpe renere energiteknologierGuangwen Zhou er professor i maskinteknik ved Binghamton University, State University of New York. Kredit:Binghamton University, State University of New York Ny forskning ledet af fakultetet ved B
Ny forskning kan hjælpe renere energiteknologierGuangwen Zhou er professor i maskinteknik ved Binghamton University, State University of New York. Kredit:Binghamton University, State University of New York Ny forskning ledet af fakultetet ved B -
 Selvsamlende materialer kan danne mønstre, der kan være nyttige i optiske enhederScanningselektronmikroskopbilleder af krystalstrukturen af blokcopolymermaterialet, illustrerer deres usædvanlige kvasikrystal symmetrier. Regioner med forskellige symmetriegenskaber er fremhævet i
Selvsamlende materialer kan danne mønstre, der kan være nyttige i optiske enhederScanningselektronmikroskopbilleder af krystalstrukturen af blokcopolymermaterialet, illustrerer deres usædvanlige kvasikrystal symmetrier. Regioner med forskellige symmetriegenskaber er fremhævet i -
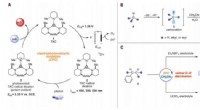 Elektrofotokatalytisk diamination af vicinale C -H -bindingerElektrofotokatalytisk amination af C -H -bindinger. (A) Generisk elektrofotokatalytisk cyklus med trisaminocyclopropenium (TAC) 1. (B) Ritter-type C-H amineringsreaktion. (C) Elektrofotokatalytiske vi
Elektrofotokatalytisk diamination af vicinale C -H -bindingerElektrofotokatalytisk amination af C -H -bindinger. (A) Generisk elektrofotokatalytisk cyklus med trisaminocyclopropenium (TAC) 1. (B) Ritter-type C-H amineringsreaktion. (C) Elektrofotokatalytiske vi -
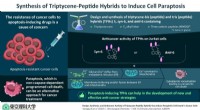 Programmeret celledød i cancerceller:Overvinde resistens gennem paraptose-inducerende forbindelserForskere fra Tokyo University of Science har udviklet nye komplekse peptidhybrider, som kan inducere en type programmeret celledød kaldet paraptose i apoptose-resistente cancerceller. Kredit:Tokyo Uni
Programmeret celledød i cancerceller:Overvinde resistens gennem paraptose-inducerende forbindelserForskere fra Tokyo University of Science har udviklet nye komplekse peptidhybrider, som kan inducere en type programmeret celledød kaldet paraptose i apoptose-resistente cancerceller. Kredit:Tokyo Uni
- Marmor og kvartsit er ikke -folierede klipper, fordi?
- Prisretfærdighed:Hvornår giver forbrugerne Michelin-manden skylden?
- Hvad er den intermolekylære kraft, der findes i svovlbrinte?
- En ny vandopdelingsteknik til at generere rent brint
- Robotter gør det muligt for bier og fisk at tale med hinanden
- Hvad er en pindes tæthed?


