Hvad er oxidationen halvreaktion for 2 mg o22mgo?
1. Identificer oxidation og reduktion:
* Oxidation: Tab af elektroner (stigning i oxidationsnummer)
* reduktion: Gevinst af elektroner (fald i oxidationsnummer)
I reaktionen 2 mg + o₂ → 2mgo:
* magnesium (mg) går fra en oxidationstilstand på 0 (elementær form) til +2 i MgO. Dette er oxidation.
* ilt (O₂) går fra en oxidationstilstand på 0 (elementær form) til -2 i MGO. Dette er reduktion.
2. Skriv oxidationen halvreaktion:
Oxidationen halvreaktion fokuserer kun på de arter, der oxideres.
* mg → mg²⁺ + 2e⁻
Forklaring:
* Magnesium (Mg) mister to elektroner for at blive en magnesiumion (mg²⁺).
* "2E⁻" repræsenterer de to elektroner, der går tabt i oxidationsprocessen.
Vigtig note: Halvreaktioner skal være afbalanceret med hensyn til både atomer og ladning. Oxidationen halvreaktion ovenfor er allerede afbalanceret.
Sidste artikelHvad er produkt af styren reagerer med brom?
Næste artikelHvad er forbindelser, der frigiver brintioner?
 Varme artikler
Varme artikler
-
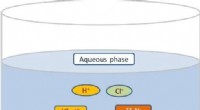 Studerer mekanismen for metalekstraktion med ioniske væskerOpløsning af ionisk flydende betainium -bis (trifluormethylsulfonyl) imid i den vandige fase starter kemiske interaktioner og fordeling af ioner mellem de to flydende faser. Kredit:J. Mol et al., Virk
Studerer mekanismen for metalekstraktion med ioniske væskerOpløsning af ionisk flydende betainium -bis (trifluormethylsulfonyl) imid i den vandige fase starter kemiske interaktioner og fordeling af ioner mellem de to flydende faser. Kredit:J. Mol et al., Virk -
 Bioinspirerede materialer-lån fra naturens legebogEt skibsskelet af havsvamp, der viser den komplekse karakter af dets struktur, som giver fantastisk styrke. Kredit:Michael Monn, Kesari Lab, Brown University Naturen giver utallige eksempler på un
Bioinspirerede materialer-lån fra naturens legebogEt skibsskelet af havsvamp, der viser den komplekse karakter af dets struktur, som giver fantastisk styrke. Kredit:Michael Monn, Kesari Lab, Brown University Naturen giver utallige eksempler på un -
 Flydende celler i en bølget mikrokanal til effektiv størrelsesbaseret cellesorteringSkematisk af størrelsesbaseret inerticellesortering i en bølgekanalenhed før det trifurcerede output. Forskellige størrelse biologiske celler kan opnå distinkt fokuseringsadfærd, som således resultere
Flydende celler i en bølget mikrokanal til effektiv størrelsesbaseret cellesorteringSkematisk af størrelsesbaseret inerticellesortering i en bølgekanalenhed før det trifurcerede output. Forskellige størrelse biologiske celler kan opnå distinkt fokuseringsadfærd, som således resultere -
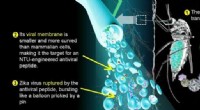 Peptid udnytter akilleshælen fra Zika-virusIllustration af forskningsresultatet. Kredit:NTU Singapore Forskere ved Nanyang Technological University, Singapore (NTU Singapore) har udviklet et antiviralt peptid, der udnytter Zika-virussen ve
Peptid udnytter akilleshælen fra Zika-virusIllustration af forskningsresultatet. Kredit:NTU Singapore Forskere ved Nanyang Technological University, Singapore (NTU Singapore) har udviklet et antiviralt peptid, der udnytter Zika-virussen ve
- Brug af systematiske metoder til at studere og forklare de sociale naturlige verdener er hensigten?
- Hvilken type erosion er der skabt oversvømmelsespladser af?
- Hvordan antibiotikaresistente mikrober beskytter sig selv mod angreb af kroppens forsvar
- Hvordan har Mars forskellige tyngdekraft end Jorden?
- Luftbårne plastpartikler tæppe fjerntliggende bjerge:undersøgelse
- Hviskerummet:Moderater på Twitter er ved at miste stemmen


