Hvad er den afbalancerede ligning for sølvnitrat og kaliumiodid?
Agno₃ (aq) + ki (aq) → Agi (s) + kno₃ (aq)
Her er en sammenbrud:
* agno₃ (aq) :Sølvnitrat, opløst i vand (vandig)
* ki (aq) :Kaliumiodid, opløst i vand (vandig)
* agi (s) :Sølv iodid, et gult bundfald (fast)
* kno₃ (aq) :Kaliumnitrat, opløst i vand (vandig)
Forklaring:
Denne reaktion er et klassisk eksempel på en dobbeltfortrængningsreaktion hvor kationerne og anionerne af reaktanterne skifter partnere.
* Sølvioner (AG⁺) fra sølvnitrat reagerer med iodidioner (i⁻) fra kaliumiodid til dannelse af sølviodid (AGI), et gult fast stof, der udfælder ud af opløsningen.
* De resterende ioner, kalium (K⁺) og nitrat (NO₃⁻), danner kaliumnitrat (Kno₃), som forbliver opløst i opløsningen.
Ligningen er afbalanceret, fordi der er lige antal af hver type atom på begge sider af ligningen:
* 1 AG på hver side
* 1 n på hver side
* 1 i på hver side
* 1 K på hver side
* 3 o på hver side
 Varme artikler
Varme artikler
-
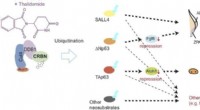 Molekylær basis for lægemiddelvirkninger på lemmer og øreudvikling afsløretThalidomid binder sig til cereblon (CRBN) og forårsager unormal lem- og øreudvikling ved at fremkalde nedbrydning af proteiner kaldet? Np63α og TAp63α gennem en proces kendt som ubiquitination. Denne
Molekylær basis for lægemiddelvirkninger på lemmer og øreudvikling afsløretThalidomid binder sig til cereblon (CRBN) og forårsager unormal lem- og øreudvikling ved at fremkalde nedbrydning af proteiner kaldet? Np63α og TAp63α gennem en proces kendt som ubiquitination. Denne -
 Hvordan en interesse for bipolar lidelse førte til en bedre forståelse af leukæmiEt nyt projekt afslører, at enzymet GSK-3, et mål for stemningslidelsen stoffet lithium, har en rolle i at kontrollere alternativ splejsning i celler. Denne observation kan give indsigt i leukæmi. Kre
Hvordan en interesse for bipolar lidelse førte til en bedre forståelse af leukæmiEt nyt projekt afslører, at enzymet GSK-3, et mål for stemningslidelsen stoffet lithium, har en rolle i at kontrollere alternativ splejsning i celler. Denne observation kan give indsigt i leukæmi. Kre -
 Økolim kan erstatte skadelige klæbemidler i træbyggeriKredit:Aalto Universitet Forskere ved Aalto Universitetet har udviklet en biobaseret klæbemiddel, der kan erstatte formaldehydholdige klæbemidler i træbyggeri. Det vigtigste råmateriale i den nye l
Økolim kan erstatte skadelige klæbemidler i træbyggeriKredit:Aalto Universitet Forskere ved Aalto Universitetet har udviklet en biobaseret klæbemiddel, der kan erstatte formaldehydholdige klæbemidler i træbyggeri. Det vigtigste råmateriale i den nye l -
 Reduktion af fælder øger ydeevnen af organiske fotodetektorerFleksible organiske fotodetektorer (OPDer) har et enormt potentiale for applikationer inden for billig billedbehandling, sundhedsovervågning og nær infrarød sensing. Kredit:Christian Körner Fysike
Reduktion af fælder øger ydeevnen af organiske fotodetektorerFleksible organiske fotodetektorer (OPDer) har et enormt potentiale for applikationer inden for billig billedbehandling, sundhedsovervågning og nær infrarød sensing. Kredit:Christian Körner Fysike


