Hvor mange atomer er der i 1 g brintgas?
1. Forstå strukturen af brintgas
* Hydrogengas findes som et diatomisk molekyle (H₂), hvilket betyder, at to brintatomer binder sammen.
2. Molmasse
* Den molære masse af brintgas (H₂) er ca. 2 g/mol (1 g/mol pr. Hydrogenatom X 2 -atomer).
3. Beregning af mol
* Opdel massen af brintgas med dens molære masse for at finde antallet af mol:
* Mol H₂ =1 g / 2 g / mol =0,5 mol
4. Avogadros nummer
* Avogadros nummer fortæller os antallet af partikler (atomer, molekyler osv.) I en mol af et stof. Det er cirka 6,022 x 10²³ partikler/mol.
5. Beregning af atomer
* Multiplicer antallet af mol brintgas med Avogadros nummer for at finde antallet af H₂ -molekyler:
* Antal H₂ -molekyler =0,5 mol * 6,022 x 10²³ molekyler/mol =3,011 x 10²³ molekyler
* Da hvert H₂ -molekyle indeholder 2 hydrogenatomer, multiplicerer antallet af molekyler med 2 for at få det samlede antal hydrogenatomer:
* Antal hydrogenatomer =3,011 x 10²³ molekyler * 2 atomer/molekyle = 6,022 x 10²³ atomer
Derfor er der ca. 6,022 x 10²³ brintatomer i 1 gram brintgas.
Sidste artikelHvorfor reagerer brom med hexen, men ikke benzen?
Næste artikelEr fluor lignende egenskaber som klor?
 Varme artikler
Varme artikler
-
 Forskere udvikler semi-flydende metalanode til næste generations batterierCarnegie Mellon-forskere har udviklet en dobbeltledende polymer/carbon-kompositmatrix med lithiummikropartikler, der kan bruges som elektrode i næste generations batterier. Kredit:Carnegie Mellon Univ
Forskere udvikler semi-flydende metalanode til næste generations batterierCarnegie Mellon-forskere har udviklet en dobbeltledende polymer/carbon-kompositmatrix med lithiummikropartikler, der kan bruges som elektrode i næste generations batterier. Kredit:Carnegie Mellon Univ -
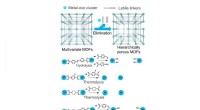 Strategier til at generere større porer i metal-organiske rammerIntroduktion af mesoporer i mikroporøse multivariate MOFer ved selektivt at fjerne labile linkere gennem hydrolyse, termolyse og ozonolyse. Gengivet fra Chem. Soc. Rev., 2019, 48, 4823-4853 med tillad
Strategier til at generere større porer i metal-organiske rammerIntroduktion af mesoporer i mikroporøse multivariate MOFer ved selektivt at fjerne labile linkere gennem hydrolyse, termolyse og ozonolyse. Gengivet fra Chem. Soc. Rev., 2019, 48, 4823-4853 med tillad -
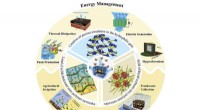 Hygroskopiske polymergeler:Opsamling af ferskvand og energi fra atmosfærisk fugtSyntesestrategier og AME-anvendelser af HPGer. Kredit:NIMTE Den globale befolkningseksplosion har udløst en enorm efterspørgsel efter ferskvand og energi. På trods af de store fremskridt inden for
Hygroskopiske polymergeler:Opsamling af ferskvand og energi fra atmosfærisk fugtSyntesestrategier og AME-anvendelser af HPGer. Kredit:NIMTE Den globale befolkningseksplosion har udløst en enorm efterspørgsel efter ferskvand og energi. På trods af de store fremskridt inden for -
 Bygge vægge, der vil gøre sommerens hedebølger mere tålelige(a) PCM-vægtværsnit (b) temperaturmålingsposition. Kredit:Korea Institute of Science and Technology (KIST) Med sommervarmen, der bliver mere og mere uudholdelig og langvarig på grund af klimaændri
Bygge vægge, der vil gøre sommerens hedebølger mere tålelige(a) PCM-vægtværsnit (b) temperaturmålingsposition. Kredit:Korea Institute of Science and Technology (KIST) Med sommervarmen, der bliver mere og mere uudholdelig og langvarig på grund af klimaændri
- Hvorfor åk er designet til lav fluxdensitet?
- Vil effekter af ulige opvarmning land og vand forårsage en tornado?
- Hvor er verdens største magma -kammer?
- Hvornår er det bedste tidspunkt på dagen at træffe en beslutning?
- Turisme hovedsageligt ansvarlig for havaffald på Middelhavets strande
- Global opvarmning øger frostskader på træer i Centraleuropa


