Hvorfor findes de fleste metaller i skorpe som forbindelser og ikke formen af elementer?
1. Reaktivitet: Metaller er generelt reaktive elementer. De har en tendens til let at miste elektroner for at danne positive ioner (kationer). Denne høje reaktivitet gør dem modtagelige for kemiske reaktioner med andre elementer i miljøet.
2. Oxygen og vand: Oxygen er et meget rigeligt element i jordens atmosfære og hydrosfære. Metaller reagerer let med ilt og danner oxider. Vand spiller også en betydelig rolle i korrosionen af metaller og danner hydroxider.
3. Stabilitet af forbindelser: Forbindelserne dannet af metaller er ofte mere stabile end de elementære former. Denne stabilitet opstår fra de stærke elektrostatiske kræfter, der holder ionerne sammen i forbindelsen.
4. Geologiske processer: Geologiske processer, såsom forvitring, erosion og hydrotermisk aktivitet, bidrager til dannelsen af metalforbindelser. Disse processer involverer interaktion mellem metaller og forskellige elementer og forbindelser, hvilket resulterer i dannelse af stabile mineraler.
Undtagelser:
Mens de fleste metaller findes som forbindelser, er der nogle få undtagelser:
* ædle metaller: Metaller som guld (AU) og platin (PT) er relativt ureaktive og findes i deres elementære form i naturen.
* indfødte metaller: Nogle metaller, såsom kobber (Cu) og sølv (AG), findes i deres oprindelige form, selvom de ofte er forbundet med andre mineraler.
Kortfattet:
Metallers reaktivitet, tilstedeværelsen af ilt og vand, stabiliteten af metalforbindelser og geologiske processer bidrager alle til forekomsten af metaller i sammensat form i jordskorpen.
 Varme artikler
Varme artikler
-
 3D-ordnet kanal forbedrer elektrokatalyseGrafisk abstrakt. Kredit:DOI:10.1021/jacs.1c04653 Et team ledet af prof. YU Shuhong og prof. HOU Zhonghuai fra University of Science and Technology of China (USTC) fra det kinesiske videnskabsakad
3D-ordnet kanal forbedrer elektrokatalyseGrafisk abstrakt. Kredit:DOI:10.1021/jacs.1c04653 Et team ledet af prof. YU Shuhong og prof. HOU Zhonghuai fra University of Science and Technology of China (USTC) fra det kinesiske videnskabsakad -
 Ny undersøgelse bekræfter bølget arkproteinstruktur forudsagt i 1953Det krusede betaark er en variation af det plisserede betaark, et velkendt strukturelt motiv, der findes i tusindvis af proteiner. Linus Pauling og Robert Corey beskrev det krusede beta-ark i 1953, me
Ny undersøgelse bekræfter bølget arkproteinstruktur forudsagt i 1953Det krusede betaark er en variation af det plisserede betaark, et velkendt strukturelt motiv, der findes i tusindvis af proteiner. Linus Pauling og Robert Corey beskrev det krusede beta-ark i 1953, me -
 Hvordan rentvandsteknologier kunne få et løft fra røntgensynkrotronerKredit:George Hodan/public domain Verden har brug for rent vand, og dets behov vil kun vokse i de kommende årtier. Alligevel er afsaltning og andre vandrensende teknologier ofte dyre og kræver meg
Hvordan rentvandsteknologier kunne få et løft fra røntgensynkrotronerKredit:George Hodan/public domain Verden har brug for rent vand, og dets behov vil kun vokse i de kommende årtier. Alligevel er afsaltning og andre vandrensende teknologier ofte dyre og kræver meg -
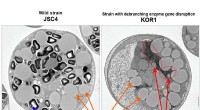 Ændring af kulhydrater til lipider til mikroalger biobrændstofferFigur 1:Elektronmikroskopbillede af lipidproduktion i mikroalgerne Chlamydomonas sp. Kredit:Kobe University Et tværinstitutionelt samarbejde har udviklet en teknik til at fordele kulstofressourcer
Ændring af kulhydrater til lipider til mikroalger biobrændstofferFigur 1:Elektronmikroskopbillede af lipidproduktion i mikroalgerne Chlamydomonas sp. Kredit:Kobe University Et tværinstitutionelt samarbejde har udviklet en teknik til at fordele kulstofressourcer
- Strategisk formulering af almindelig cement kan have stor indflydelse på vandrensning
- Kvantekommunikation bliver tynd og let
- Måling af temperatur på havbunden for millioner år siden kan vise, om havets opvarmning øger met…
- Ny geologisk undersøgelse viser, at Skandinavien blev født i Grønland
- Sproglige ændringer i køn og etniske stereotyper korrelerede med store sociale bevægelser og demo…
- MITs Robogami vil have dig til at tilpasse origami-inspireret,


