Lithium valenselektroner type ioner dannet?
* Valenselektroner: Lithium (Li) har en valenselektron i sin yderste skal.
* iondannelse: Lithium mister let sin enkelt valenselektron for at opnå en stabil, fyldt elektronskal som helium. Dette resulterer i dannelsen af A positivt ladet ion kaldes en lithiumkation (Li+) .
Nøglepunkter
* metaller Ligesom lithium har en tendens til at * miste * elektroner for at blive kationer.
* ikke -metaller har tendens til at * få * elektroner til at blive anioner.
* Gebyret på en ion afspejler antallet af mistede elektroner eller opnået.
Sidste artikelEr dinitrogen hexaiodidionisk eller molekylær?
Næste artikelHvad er ligningen for tilsætning af brom til Pentene?
 Varme artikler
Varme artikler
-
 Fremtidens plastik vil leve mange tidligere liv takket være kemisk genbrugDetaljebillede af genbrugsplast. Kredit:Patrick Campbell / University of Colorado Boulder En dag i en ikke alt for fjern fremtid kan plastikken i vores satellitter, biler og elektronik alle leve de
Fremtidens plastik vil leve mange tidligere liv takket være kemisk genbrugDetaljebillede af genbrugsplast. Kredit:Patrick Campbell / University of Colorado Boulder En dag i en ikke alt for fjern fremtid kan plastikken i vores satellitter, biler og elektronik alle leve de -
 Effektivt materiale udviklet til at forhindre post-kirurgisk vedhæftning(a) De levende celler uden for 1 μL prikken i PEC angiver, at materialet ikke skaber et giftigt miljø (målestreg:500 μm). Dette tyder på, at materialet hæmmer levedygtighed, når celler er knyttet dire
Effektivt materiale udviklet til at forhindre post-kirurgisk vedhæftning(a) De levende celler uden for 1 μL prikken i PEC angiver, at materialet ikke skaber et giftigt miljø (målestreg:500 μm). Dette tyder på, at materialet hæmmer levedygtighed, når celler er knyttet dire -
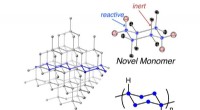 Ny polymer inspireret af krystallinsk silicium til at bygge bedre computere og solcellerAt finde nye måder at lave bedre materialer til elektroniske kredsløb på er en måde at lave en bedre enhed. En ny polymer, kaldet poly (cyclosilane) (nederst til højre), er i det væsentlige en ultra-l
Ny polymer inspireret af krystallinsk silicium til at bygge bedre computere og solcellerAt finde nye måder at lave bedre materialer til elektroniske kredsløb på er en måde at lave en bedre enhed. En ny polymer, kaldet poly (cyclosilane) (nederst til højre), er i det væsentlige en ultra-l -
 Binde molekyler lige så let som snørebåndEksempler på molekylære noder undersøgt. Kredit:UNIGE Selvom knuder kan være til gene, de er også meget nyttige, når det kommer til at binde dine snørebånd, eller når du skal sejle. I matematik, d
Binde molekyler lige så let som snørebåndEksempler på molekylære noder undersøgt. Kredit:UNIGE Selvom knuder kan være til gene, de er også meget nyttige, når det kommer til at binde dine snørebånd, eller når du skal sejle. I matematik, d
- Undersøgelse skinner lys over alternative medicinske billeddannelsesteknikker
- Forskere designer tilpassede nanopartikler med ny stencilmetode
- Isolatorer tilbyder modstand mod strømmen af elektrisk strøm.?
- Video:Besøg et Mars-robottestlaboratorium
- Hvad skal man vide om den vellykkede redning af en amerikansk forsker, der var fanget i en dyb tyrki…
- Hvor tungt er et rumfartøj?


