Hvor mange mol bromidioner er til stede i 750,0 ml 1,35 M MGBR2?
1. Forstå formlen:
* MGBR₂ er magnesiumbromid. Det adskiller sig i opløsning til dannelse af en mg²⁺ ion og to br⁻ioner:
Mgbr₂ (aq) → mg²⁺ (aq) + 2br⁻ (aq)
2. Beregn mol af mgbr₂:
* Vi får volumen (750,0 ml) og molaritet (1,35 m) af MGBR₂ -opløsningen.
* Konverter volumen til liter:750,0 ml * (1 l / 1000 ml) =0,750 L
* Brug molaritetsformel til at finde mol:
Moles =molaritet * volumen
Mol =1,35 mol/l * 0,750 l =1,0125 mol mgBr₂
3. Beregn mol af bromidioner:
* Fra den afbalancerede ligning ser vi, at 1 mol mgBr₂ producerer 2 mol br⁻ioner.
* Derfor mol af br⁻ =1,0125 mol mgbr₂ * (2 mol br⁻ / 1 mol mgbr₂) =2,025 mol br⁻
Svar: Der er 2.025 mol af bromidioner til stede i 750,0 ml 1,35 M MGBR₂ opløsning.
 Varme artikler
Varme artikler
-
 Forskere designer en forbedret vej til kulstofneutral plastFengwang Li demonstrerer den kobberbaserede katalysator, som han og hans samarbejdspartnere har designet. Placeret i en elektrolysator, katalysatoren er i stand til effektivt at omdanne affalds-CO2 di
Forskere designer en forbedret vej til kulstofneutral plastFengwang Li demonstrerer den kobberbaserede katalysator, som han og hans samarbejdspartnere har designet. Placeret i en elektrolysator, katalysatoren er i stand til effektivt at omdanne affalds-CO2 di -
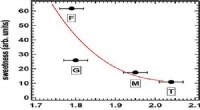 Vand kan være nøglen til at forstå sødmeKredit:American Chemical Society Et tranebær, honning eller en slikbar - hvad smager sødest? Disse fødevarer indeholder sukkerarter, som mennesker kan opfatte forskelligt. Et tranebær virker syrli
Vand kan være nøglen til at forstå sødmeKredit:American Chemical Society Et tranebær, honning eller en slikbar - hvad smager sødest? Disse fødevarer indeholder sukkerarter, som mennesker kan opfatte forskelligt. Et tranebær virker syrli -
 Forskere udvikler ultrastærke aerogeler med materialer, der bruges i skudsikre vesteAerogelerne har ønskværdige egenskaber såsom letvægts, semi-transparent og høj belastningsbærende evne. Kredit:University of Hong Kong Aerogeler er lette materialer med omfattende porer i mikroskal
Forskere udvikler ultrastærke aerogeler med materialer, der bruges i skudsikre vesteAerogelerne har ønskværdige egenskaber såsom letvægts, semi-transparent og høj belastningsbærende evne. Kredit:University of Hong Kong Aerogeler er lette materialer med omfattende porer i mikroskal -
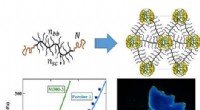 Polymerer, der efterligner kamæleons hudØverst til venstre:molekylær struktur af en plastomer syntetiseret i dette værk; højre:supramolekylær struktur dannet ved samling af identiske plastomerer. Nederst-til venstre:belastningskurver til pl
Polymerer, der efterligner kamæleons hudØverst til venstre:molekylær struktur af en plastomer syntetiseret i dette værk; højre:supramolekylær struktur dannet ved samling af identiske plastomerer. Nederst-til venstre:belastningskurver til pl
- Hvorfor kan farven på phenolphtalein langsomt forsvinde, selv efter at al syre er titreret?
- Hvordan det indre ur i vores celler påvirkes af mekaniske kræfter
- Hvilket forklarer bedst, hvorfor vind opstår?
- Overpris? Forskere forklarer kunstige prisstigninger i taxa-appen Uber
- Hvordan medlemmer af mikrobiomet specifikt bekæmper Salmonella-infektioner
- Forhistoriske megaoversvømmelser mindre end antaget


