Hvad er den komplette ioniske ligning for blynitrat og kaliumsulfat?
1. Skriv den afbalancerede molekylære ligning:
Pb (no₃) ₂ (aq) + k₂so₄ (aq) → pbso₄ (s) + 2kno₃ (aq)
2. Identificer de opløselige ioniske forbindelser:
* Blynitrat (Pb (No₃) ₂) er opløseligt i vand.
* Kaliumsulfat (k₂so₄) er opløseligt i vand.
* Kaliumnitrat (kno₃) er opløseligt i vand.
* Bly sulfat (PBSO₄) er uopløselig i vand.
3. Adskil de opløselige ioniske forbindelser i deres ioner:
* Pb (no₃) ₂ (aq) → pb²⁺ (aq) + 2no₃⁻ (aq)
* K₂so₄ (aq) → 2k⁺ (aq) + so₄²⁻ (aq)
* 2Kno₃ (aq) → 2k⁺ (aq) + 2no₃⁻ (aq)
4. Skriv den komplette ioniske ligning:
Pb²⁺ (aq) + 2no₃⁻ (aq) + 2k⁺ (aq) + so₄²⁻ (aq) → pbso₄ (s) + 2k⁺ (aq) + 2no₃⁻ (aq)
Vigtig note: Det faste produkt (PBSO₄) forbliver som en enkelt enhed i ligningen, fordi det ikke adskiller sig i ioner i opløsning.
 Varme artikler
Varme artikler
-
 Måling af spændingen i en celle med et molekyleKunstnerens syn på en lipidmembran markeret med FliptR-molekylet. Lipiderne er blå (hydrofil del) og gule (hydrofob del). Når lipider strækkes (venstre del) har molekylet en kort levetid (grøn), hvori
Måling af spændingen i en celle med et molekyleKunstnerens syn på en lipidmembran markeret med FliptR-molekylet. Lipiderne er blå (hydrofil del) og gule (hydrofob del). Når lipider strækkes (venstre del) har molekylet en kort levetid (grøn), hvori -
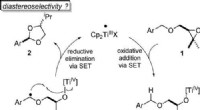 Forskere udvikler en bæredygtig katalyseprocesAtomøkonomisk omdannelse af benzylethere til acetaler ved titanocen(III)-katalyse i enkeltelektrontrin (SET). Angewandte Chemie, DOI:10.1002/anie.202013561 Acetaler er vigtige kemiske forbindelser
Forskere udvikler en bæredygtig katalyseprocesAtomøkonomisk omdannelse af benzylethere til acetaler ved titanocen(III)-katalyse i enkeltelektrontrin (SET). Angewandte Chemie, DOI:10.1002/anie.202013561 Acetaler er vigtige kemiske forbindelser -
 Økologiske polymerscintillatorer begejstrer røntgensamfundetAmorfe polymerscintillatorer, der udviser flere radioluminescensfarver, vil bidrage til røntgenbilleder i høj opløsning. Kredit:Wei et al., doi 10.1117/1.AP.4.3.035002. Røntgendetektion er af stor
Økologiske polymerscintillatorer begejstrer røntgensamfundetAmorfe polymerscintillatorer, der udviser flere radioluminescensfarver, vil bidrage til røntgenbilleder i høj opløsning. Kredit:Wei et al., doi 10.1117/1.AP.4.3.035002. Røntgendetektion er af stor -
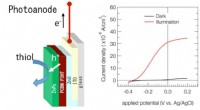 Miljøvenlige elektrokemiske katalysatorer, der bruger solceller til at høste energi fra solenStrukturen af den foreslåede enhed, viser, hvordan de genererede huller (h+) bruges til at lette thioloxidation. Den målte strøm stiger dramatisk under belysning og anvendelse af et lille potentiale
Miljøvenlige elektrokemiske katalysatorer, der bruger solceller til at høste energi fra solenStrukturen af den foreslåede enhed, viser, hvordan de genererede huller (h+) bruges til at lette thioloxidation. Den målte strøm stiger dramatisk under belysning og anvendelse af et lille potentiale
- Spækhuggere angriber skibe igen:Her er en historie om praksis
- Amerikanske stater droner inspicerer broer, hjælpe med at forudsige laviner
- Hvem er den berømte ruminnovator?
- Visualisering af funktionelle komponenter for at karakterisere optimale kompositelektroder
- Langsigtet undersøgelse viser hurtig dannelse af mikro- og nanoplast i miljøet
- Minnesota-forskere opdager, hvordan elektricitet bevæger sig gennem celler


