Når et bariumatom danner sin mest almindelige ion det?
Her er hvorfor:
* Elektronkonfiguration: Barium (BA) har en elektronkonfiguration af [XE] 6S². Dette betyder, at det har to elektroner i sin yderste skal.
* octet regel: Atomer har en tendens til at vinde, miste eller dele elektroner for at opnå en stabil elektronkonfiguration, normalt med otte elektroner i deres yderste skal (oktetreglen).
* ionisk binding: Barium er et metal, og metaller har en tendens til at miste elektroner til dannelse af positive ioner (kationer). For at opnå en stabil oktet mister Barium let sine to ydre skalelektroner.
Derfor er den mest almindelige ion af barium ba²⁺ .
Sidste artikelHvad er formlen for kviksølv I -oxid og II -oxid?
Næste artikelHvad er de fysiske egenskaber ved natriumhydrogencarbonat?
 Varme artikler
Varme artikler
-
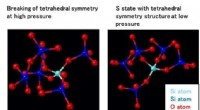 Strukturel oprindelse af de unormale egenskaber af SiO2-glas under trykStrukturelle træk ved SiO2-glas under tryk. / Translationel rækkefølge i SiO2-glas som funktion af parameteren z opnået i vores eksperiment med MD-RMC-modellering og MD-simulering med BKS-model ved 0
Strukturel oprindelse af de unormale egenskaber af SiO2-glas under trykStrukturelle træk ved SiO2-glas under tryk. / Translationel rækkefølge i SiO2-glas som funktion af parameteren z opnået i vores eksperiment med MD-RMC-modellering og MD-simulering med BKS-model ved 0 -
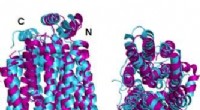 Ny forskning transformerer glukosetransportproteiner til vandopløselig formTo vinkler af den krystallinske struktur GLUT1 (magenta) glucosetransporterprotein overlejret med den AlphaFold2 computerforudsagte vandopløselige variant af det samme protein (cyan) viser, at det kry
Ny forskning transformerer glukosetransportproteiner til vandopløselig formTo vinkler af den krystallinske struktur GLUT1 (magenta) glucosetransporterprotein overlejret med den AlphaFold2 computerforudsagte vandopløselige variant af det samme protein (cyan) viser, at det kry -
 En ny teknik til at producere billigere og mere effektiv klorFigur 1:Karakterisering af Pt1/CNT-katalysator omfattende atomisk dispergerede Pt?N4-steder på overfladen af CNT. Kredit:UNIST Klor er et af de mest udbredte industrielle kemikalier i verden i d
En ny teknik til at producere billigere og mere effektiv klorFigur 1:Karakterisering af Pt1/CNT-katalysator omfattende atomisk dispergerede Pt?N4-steder på overfladen af CNT. Kredit:UNIST Klor er et af de mest udbredte industrielle kemikalier i verden i d -
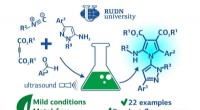 Kemiker foreslår miljøvenlig syntese af fluorescerende forbindelser til medicinKredit:RUDN Universitet En kemiker fra RUDN og Shahid Beheshti University(SBU) foreslog en miljøvenlig metode til syntese af pyrrol- og pyrazolderivater med en bred vifte af anvendelser inden for
Kemiker foreslår miljøvenlig syntese af fluorescerende forbindelser til medicinKredit:RUDN Universitet En kemiker fra RUDN og Shahid Beheshti University(SBU) foreslog en miljøvenlig metode til syntese af pyrrol- og pyrazolderivater med en bred vifte af anvendelser inden for
- Karakteriserer strukturen af selvsamlende organiske molekyler på overfladen af nanopartikler
- Hvorfor energi skabt af øjeblik eller bevægelse?
- Forskere omdanner opfangede drivhusgasser til cykliske karbonater med biomassederivater
- Produktion af ammoniak gennem elektrokemiske processer kan reducere kuldioxidemissioner
- Hvilke variabler bruger du til at beregne acceleration?
- Hvad er momentumet på 4 kg kugle, der bevæger sig med hastighed 2 ms?


